Primuline
La primuline est un colorant formé à partir du système cyclique benzothiazole.
| Primuline | |
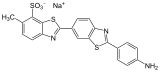
| |
| Identification | |
|---|---|
| Nom UICPA | sodium;2-[2-(4-aminophenyl)-1,3-benzothiazol-6-yl]-6-methyl-1,3-benzothiazole-7-sulfonate |
| Synonymes |
Direct Yellow 7, Carnotine, C.I. 49010 |
| No CAS | |
| No ECHA | 100.030.698 |
| No CE | 233-781-3 |
| PubChem | |
| ChEBI | 90399 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C21H15N3O3S3 |
| Masse molaire[1] | 453,557 ± 0,034 g/mol C 55,61 %, H 3,33 %, N 9,26 %, O 10,58 %, S 21,21 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Les primulines sont considérées comme des dérivés de la déhydrothiotoluidine (aminobenzényltoluylmercaptan), obtenue lorsque la para-toluidine est chauffée avec du soufre pendant dix-huit heures à 180-190 ° C, puis pendant six heures supplémentaires à 200-220 ° C. Le déhydrothiotoluidine n’est pas lui-même un colorant, mais si le chauffage est effectué à une température plus élevée en présence de plus de soufre, alors une base se forme, qui donne du jaune de primuline lors de la sulfonation[2].
Le jaune de primuline est un mélange de sels de sodium et contient probablement au moins trois cycles thiazole en combinaison. C'est une teinture de coton substantielle de nuance plutôt fugitive, mais qui peut être diazotée sur la fibre puis développée avec d'autres composants, donnant une série de couleurs enracinées.
La primuline est généralement disponible sous forme de sel de sodium. Elle a aussi des propriétés fluorescentes.
La thioflavine T est obtenue par méthylation de la déshydrothiotoluidine avec du méthanol en présence d'acide chlorhydrique. La thioflavine S résulte de la méthylation de la déshydrothiotoluidine avec de l'acide sulfonique. Cet acide sulfonique sur oxydation avec de la poudre décolorante ou avec du peroxyde de plomb, en solution alcaline, donne du jaune de chloramine, qui teint le coton d'un beau jaune.
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Arthur George Green, « N/A », J. Soc. Chem. Ind., vol. 1, , p. 194