Pile à bactéries
Une pile microbienne (ou biopile ou pile à bactéries) est une pile basée sur le principe des piles à combustible[1]: la cathode est alimentée en oxygène (en général par l'air) et l'anode est constituée d'une électrode placée au sein d'une chambre contenant un biofilm de bactéries et de quoi les nourrir.
Elles sont également désignées par l'acronyme MFC provenant de la dénomination anglo-saxonne : microbial fuel cell (littéralement : Pile à combustible microbienne).
Principe
Les molécules carbonées produites par les êtres vivants le sont sous des formes réduites qui peuvent être oxydées sous l'action du dioxygène de l'air. La chaîne respiratoire des êtres vivants est d'ailleurs basée sur ce principe.
Il est donc possible de produire de l'énergie à partir de molécules carbonées. Il existe des piles fonctionnant sans bactéries, basée sur l'oxydation spontanée du glucose. Mais la bactérie grâce à son cycle catalytique, peut spectaculairement augmenter la cinétique de la réaction, et fournir des intensités surfaciques supérieures au mA.cm-2[2]. Elle joue un rôle de biocatalyseur en échangeant des électrons avec le matériau d’une électrode, en utilisant des réactions issues de son métabolisme. Les bactéries qui ont ces capacités sont dites « électrochimiquement actives » ou « électroactives ».
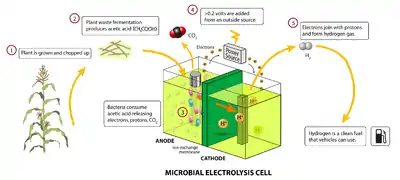
Tandis que les piles à bactéries produisent un courant électrique à partir de la décomposition microbienne de composés organiques, les cellules d'électrolyse microbienne inversent en partie le processus pour générer de l'hydrogène ou du méthane à partir de matière organique en y appliquant un courant électrique[3].
Électrode
Elle est constituée de carbone, graphite, inox, platine ou carbone vitreux réticulé peut avoir diverses formes (fil, grille, feuille (chiffonnée), plaque, structure conductrice en éponge ou feutre voire en granules, etc.). L’objectif est d’avoir une aire de contact avec le biofilm aussi vaste que possible.
Membrane séparatrice échangeuse de protons
Elle évite le mélange de l'anolyte et du catholyte (s'ils sont différents) et empêche les produits de réaction d'une électrode de s'acheminer vers l'autre électrode.
Les membranes Nafion et Ultrex sont parmi les plus utilisées dans les piles microbiennes.
Transfert d'électrons
Trois mécanismes de transfert d'électrons de la bactéries aux électrodes sont connus :
- transfert direct, il s'agit du contact physique entre la membrane cellulaire de la bactérie et l'électrode. L'électron est transporté par des complexes transporteurs d’électrons liés à la membrane bactérienne (ex : cytochromes)[4] - [5] ;
- transfert indirect, via des médiateurs exogènes tels que du rouge neutre[6] ou des médiateurs endogènes propres à la bactérie (ex : phénazines[7] ;
- transfert via des pili aussi dits « nanowires » qui font un pont conducteur entre l'électrode (ou d'autres cellules bactériennes) et la bactérie[8].
Recherche, prototypes
En 2009, la recherche avance sur ce sujet[9].
En 2014 un premier prototype français était limité (faible puissance et instabilité). Ces problèmes étaient en grande partie résolus en 2017[10].
Utilisations possibles
Cette réaction, qui pourrait - éventuellement dans le cadre d'un processus de chimie verte - permettre de produire de l'énergie à partir de déchets organiques[11] - [12] - [13] - [14] - [15] - [16], d'eaux sales ou d'autres substrats pollués ou riches en bactéries, suscite de l'intérêt[17].
Alternatives proches
Le méthanol, les acides organiques, le glucose[18] voire la cellulose[19] peuvent aussi servir de carburant pour le fonctionnement de piles.
Références
- Monier J.M. ; Haddour N. ; Niard L. ; Vogel T. et Buret F. Les biopiles - La revue 3 EI, n° 47, décembre 2006
- Fritz Scholz, Uwe Schröder, « bacterial batteries », nature biotechnology, 21, 1151-1152
- (en) Badwal, « Emerging electrochemical energy conversion and storage technologies », Frontiers in Chemistry, vol. 2, , p. 79 (PMID 25309898, PMCID 4174133, DOI 10.3389/fchem.2014.00079, Bibcode 2014FrCh....2...79B).
- Holmes, D.E., Bond, D.R., Lovley, D.R., 2004. Electron transfer by Desulfobulbus propionicus to Fe (III) and graphite electrodes. Appl. Environ. Microbiol. 70(2), 1234- 1234.
- Chang IS, Hyunsoo M, Orianna B, Jae KJ, Ho IP, Kenneth HN, Byung HK (2006). Electrochemically Active Bacteria (EAB) and Mediator-Less Microbial Fuel Cells. Journal of Microbiology and Biotechnology.16(2):163-177.
- Park DH, Laivenieks M, Guettler MV, Jain MK, Zeikus JG (1999) Microbial utilization of electrically reduced neutral red as the sole electron donor for growth and metabolite production. Appl. Environ. Microbiol. 65(7):2919-2917.
- Rabaey K, Boon N, Siciliano SD, Verhaege M, Verstraete W (2004) Biofuel cells select for microbial consortia that self-mediate electron transfer. Appl. Environ. Microbiol. 70(9):5373- 5382.
- Gorby Y, et al. (2006) Electrically conductive bacterial nanowires produced by Shewanella oneidensis strain MR-1 and other microorganisms. PNAS. 103(30):11358-11363 .
- Cercado Quezada B (2009) Traitement de déchets issus de l'industrie agro-alimentaire par pile à combustible microbienne (Doctoral dissertation, Institut National Polytechnique de Toulouse).
- « Production d’électricité : quand des enzymes rivalisent avec le platine », sur techniques-ingenieur.fr,
- Liu H, Ramnarayanan R, Logan BE (2004) Production of electricity during wastewater treatment using a single chamber microbial fuel cell. Environ. Sci. Technol. 38(7):2281-2285.
- Lefebvre O, Al-Mamun A, Ng HG (2007) A compact and cost-effective microbial fuel cell for treatment of domestic and acetate wastewater. 11th IWA World Congress on Anaerobic Digestion. 23-27 September. Brisbane, Australia
- Logan B (2005) Simultaneous wastewater treatment and biological electricity generation. Water Science & Technology. 52(1-2):31-37
- Min B, Logan BE (2004) Continuous electricity generation from domestic wastewater and organic substrates in a flat plate microbial fuel cell. Environ. Sci. Technol. 38(21):5809-5814.
- Oh SE, Logan B (2005) Hydrogen and electricity production from a food processing wastewater using fermentation and microbial fuel cell technologies. Water Res. 39:4673- 4682.
- Wang X, Feng YJ, Lee H (2007) Electricity production from beer brewery wastewater using single chamber microbial fuel cell. 11th IWA World Congress on Anaerobic Digestion. 23-27 September. Brisbane, Australie
- Hong Liu, Ramanathan Ramnarayanan, Bruce E. Logan, « production of electricity during wastewater treatment using a single chamber microbial fuel » environ. sci. technol. 38, 2281-2885
- Eugenii Katz, Andrew N. Shipway and Itamar Willner « Biochemical fuel cells », Handbook of fuel cells-fundamentalsn technology and application
- J.Niessen, U. Schröder, F. Harnisch and F. Scholtz « Gaining electricity from in situ oxydation of hydrogen produced by fermentative cellulose degradation » Letters in applied microbiology 41, 286-290
Voir aussi
Article connexe
Liens externes
Bibliographie
- Cercado Quezada B (2009) Traitement de déchets issus de l'industrie agro-alimentaire par pile à combustible microbienne
- Feron, D., & Bergel, A. (2007). Piles à combustible utilisant des enzymes et des biofilms comme catalyseurs. Techniques de l'ingénieur. Bioprocédés, (RE89).
- Lepage, G. (2012). Caractérisation et optimisation d'une pile à combustible microbienne (Doctoral dissertation, Grenoble).
- Cerdado Quezad, Bibiana (2009) PAC microbienne, Thèse de doctorat en Génie des Procédés et de l'Environnement (Institut National Polytechnique de Toulouse).
- Parot S (2007) Biofilms électroactifs : Formation, caractérisation et mécanismes. Thèse doctoral. Institut National Polytechnique de Toulouse. Toulouse, Fra. 247p.
- Parot S, Delia ML, Bergel A (2008) Forming electrochemically active biofilms from garden compost under chronoamperometry. Bioresour. Technol. 99:4809-4816.