Nombre quantique
Les nombres quantiques sont des ensembles de nombres définissant l'état quantique d'un système. Chacun de ces nombres définit la valeur d'une quantité conservée dans la dynamique d'un système quantique. Ce sont des nombres entiers ou demi-entiers, de sorte que les grandeurs observables correspondantes sont quantifiées et ne peuvent prendre que des valeurs discrètes : c'est une différence fondamentale entre la mécanique quantique et la mécanique classique, dans laquelle toutes ces grandeurs peuvent prendre des valeurs continues.
En physique des particules, les nombres quantiques dits « intrinsèques » sont des caractéristiques de chaque type de particule élémentaire. Par exemple, les nombres quantiques des électrons peuvent être définis comme les ensembles de valeurs numériques solutions de l'équation de Schrödinger pour l'atome d'hydrogène. L'état quantique des électrons des atomes est entièrement défini par quatre nombres quantiques généralement notés n, ℓ, mℓ et ms, mais chaque système quantique est décrit par un ensemble de nombres quantiques qui lui est propre, de sorte qu'on ne peut dresser de liste exhaustive des nombres quantiques.
En effet, la dynamique d'un système quantique est décrite par un opérateur hamiltonien quantique, noté H. Il existe au moins un nombre quantique correspondant à l'énergie du système quantique, c'est-à-dire de l'état satisfaisant l'équation aux valeurs propres de l'hamiltonien. Il existe également autant d'autres nombres quantiques qu'il y a d'opérateurs indépendants qui commutent avec l'hamiltonien ; comme il existe généralement plusieurs ensembles d'opérateurs indépendants pour un même système, il existe également plusieurs jeux de nombres quantiques pouvant décrire un même système.
Exemple : modèle de Hund-Mulliken des électrons dans les atomes
Plusieurs modèles quantiques ont été proposés pour décrire le comportement des électrons dans les atomes, mais le principal d'entre eux est la théorie de l'orbitale moléculaire de Friedrich Hund et Robert Mulliken à partir des travaux d'Erwin Schrödinger, John Slater et John Lennard-Jones. Cette nomenclature intègre les niveaux d'énergie du modèle de Bohr, la théorie des orbitales de Hund-Mulliken, et l'observation du spin de l'électron à l'aide de la spectroscopie et des règles de Hund[1].
Ce modèle décrit les électrons d'un atome à l'aide de quatre nombres quantiques n, ℓ, mℓ et ms, et cette nomenclature est également utilisée dans la description classique de l'état quantique des nucléons, c'est-à-dire des protons et des neutrons constituant les noyaux atomiques. La description quantique des orbitales moléculaires fait appel à d'autres nombres quantiques car l'hamiltonien et ses symétries y sont très différents.
Nombres quantiques de l'électron dans le modèle de Hund-Mulliken Nom Symbole Analogie classique Intervalle de valeurs Nombre quantique principal n Niveau d'énergie de l'électron dans l'atome 1, 2, 3, 4, etc. Nombre quantique azimutal ℓ Moment angulaire orbital de l'électron 0, 1, 2, ... n – 1 Nombre quantique magnétique mℓ Projection du moment angulaire orbital sur un axe – ℓ, ... 0, ... ℓ Nombre quantique magnétique de spin ms Projection du moment angulaire intrinsèque (spin) de l'électron – 12 ou + 12
Nombre quantique principal n
Le nombre quantique principal, noté n, identifie la couche électronique et correspond au niveau d'énergie de l'électron dans l'atome. Les valeurs de n sont entières et strictement positives[2], c'est-à-dire que n = 1, 2, 3, 4, etc..
Le nombre n est également le rang de la n-ième valeur propre de l'équation de Schrödinger indépendante du temps, dite également « équation des états stationnaires » : H |φn⟩ = En |φn⟩, où φn est l'état quantique associé et En est l'énergie correspondante en ignorant le terme dépendant du moment angulaire J2. Il n'est par conséquent lié qu'à la distance radiale r par rapport au noyau atomique, de sorte que l'éloignement moyen de l'électron croît avec n : on parle de couches électroniques successives.
Nombre quantique azimutal ℓ
Le nombre quantique azimutal, noté ℓ, indique la sous-couche électronique et correspond au moment angulaire orbital de l'électron à travers la relation :
- L2 = ℏ2 ℓ (ℓ + 1).
Les valeurs de ℓ sont entières, positives et strictement inférieures à n, c'est-à-dire que ℓ = 0, 1, 2, ... n – 1[3].
En chimie et en spectroscopie, les valeurs 0, 1, 2 et 3 de ℓ correspondent respectivement à des sous-couches notées s, p, d et f. Ce nombre quantique est lié à la géométrie de la fonction d'onde de l'électron dans l'atome, ce qui influence les propriétés chimiques de cet atome ainsi que les angles de liaison avec d'autres atomes.
Nombre quantique magnétique mℓ
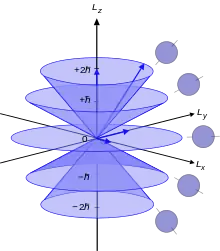
Le nombre quantique magnétique, noté mℓ, identifie l'orbitale atomique et correspond à la projection du moment angulaire orbital sur un axe donné :
- Lz = mℓ ℏ.
Les valeurs de mℓ sont entières et comprises entre – ℓ et + ℓ [4]. Ainsi les sous-couches s, identifiées par ℓ = 0, n'ont qu'une seule orbitale, tandis que sous-couches p, identifiées par ℓ = 1, comptent trois orbitales (pour mℓ = – 1, 0 et 1), les sous-couches d, identifiées par ℓ = 2, en comptent cinq (pour mℓ = – 2, – 1, 0, 1 et 2), etc.
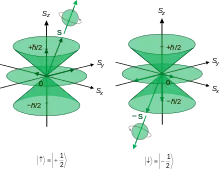
Nombre quantique magnétique de spin ms
Le nombre quantique magnétique de spin, noté ms, identifie l'électron dans son orbitale atomique et correspond à la projection du moment angulaire intrinsèque de l'électron sur un axe donné :
- Sz = ms ℏ.
Ses valeurs sont comprises entre – s et + s avec un pas entier, où s est le spin de la particule ; s vaut 12 dans le cas de l'électron, dont il est une propriété intrinsèque, de sorte que ms = ± 12 [5]. Dans la mesure où deux électrons ne peuvent avoir leurs quatre nombres quantiques égaux deux à deux en vertu du principe d'exclusion de Pauli, chaque orbitale atomique ne peut contenir que deux électrons, de nombres quantiques magnétiques de spin opposés.
Exemple de jeu de nombres quantiques alternatifs
Si l'on tient compte de l'interaction spin-orbite, les opérateurs L et S ne commutent plus avec l'opérateur hamiltonien H, et leurs valeurs propres varient en fonction du temps. Il est alors nécessaire d'utiliser un autre jeu de nombres quantiques, parmi lesquels les nombres détaillés ci-dessous[3] - [6].
Nombre quantique de moment angulaire total j

Le nombre quantique de moment angulaire total, noté j, représente la somme des moments angulaires orbital ℓ (nombre quantique azimutal) et intrinsèque s (spin de l'électron). Il vaut j = | ℓ ± s | et vérifie | mℓ + ms | ≤ j. Il quantifie le moment angulaire total J de l'électron à travers la relation :
- J = √j (j + 1) ℏ.
Projection du moment angulaire total mj
La projection du nombre quantique de moment angulaire total j sur un axe donné est quantifiée par le nombre mj, qui peut prendre toutes les valeurs espacées d'un pas entier comprises entre – j et j, et vérifie:
Parité P
La parité est la valeur propre d'une réflexion : elle est positive (+ 1) pour les états quantiques caractérisés par un nombre quantique azimutal ℓ pair, et est négative (– 1) pour les états quantiques caractérisés par un nombre ℓ impair. On parle respectivement d'une parité paire et impaire.
- P = (– 1)ℓ.
Notes et références
- (en) R. E. Dickerson, I. Geis, Chemistry, Matter, and the Universe, W. A. Benjamin Inc. (USA), 1976. (ISBN 0-19-855148-7)
- (en) A. Beiser, Concepts of Modern Physics, 4e édition, Physics, McGraw-Hill (International), 1987. (ISBN 0-07-100144-1)
- (en) P. W. Atkins, Molecular Quantum Mechanics Parts I and II: An Introduction to Quantum Chemistry (Volume 1), Oxford University Press, 1977. (ISBN 0-19-855129-0)
- (en) R. Eisberg, R. Resnick, Quantum Physics of Atoms, Molecules, Solids, Nuclei, and Particles, 2e édition, John Wiley & Sons, 1985. (ISBN 978-0-471-87373-0)
- (en) Y. Peleg, R. Pnini, E. Zaarur, E. Hecht, Quantum Mechanics, 2e édition, Schuam's Outlines, McGraw Hill (USA), 2010. (ISBN 978-0-07-162358-2)
- (en) P. W. Atkins, Molecular Quantum Mechanics Part III: An Introduction to QUANTUM CHEMISTRY (Volume 2), Oxford University Press, 1977.