Histone H2A
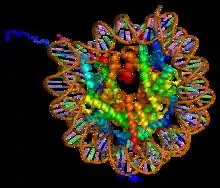
L'histone H2A est l'un des cinq types de protéines histones qui font partie de la structure de la chromatine des cellules eucaryotes. L'histone H2A est trouvée dans l'octamère de nucléosomes qui constituent la chromatine[1]. Dans chaque octamère il existe deux copies de cette histone, qui s'associent à l'histone H2B[2]. H2A est considérée comme histone "de cœur", avec H2B, H3 and H4. La formation de la particule de cœur survient en premier lieu lors de l'interaction entre deux molécules H2A[2].
Les variantes de séquence
L'histone H2A présente des variantes non alléliques[3]. Le terme "histone H2A" est générique; parmi ses variantes les plus notables, qui ne diffèrent que par quelques acides aminés, on trouve H2A.1, H2A.2, H2A.X, H2A.Z, H2A.Bbd (macroH2A)[4].
Dans les cellules différenciées la composition des variantes présentes varie. Cette situation a été observée dans les neurones en différenciation ; les changements dans la composition des variantes affectent l'histone H2A.1, et la seule variante qui reste constante au cours de la différenciation neuronale est l'histone H2AZ[3]. La variante H2AZ est échangée contre la variante de l'octamère classique H2A; cette variante est importante pour le silençage génique[5].
De récentes recherches suggèrent qu'H2AZ est incorporé dans le nucléosome à l'aide de Swr1, qui est un adenosine triphosphatase liée à Swi2/Snf2 qui fait partie d'un complexe enzymatique[6].
Une autre variante de H2A identifiée est H2AX. Cette variante a une extension ou queue C-terminale qui est utilisée pour la réparation de l'ADN. La méthode de réparation qui utilise cette variante est l'union des extrémités non homologues. Les dommages directs à l'ADN peuvent induire des changements dans les variantes de séquence. Les expériences réalisées avec des rayonnements ionisants ont associé la γ-phosphorylation de H2AX avec des cassures de l'ADN double-brin[7]. Une grande quantité de la chromatine est impliquée dans chaque coupure double brin; et une réponse aux dommages de l'ADN est la formation de foci γ-H2AX.
La variante MacroH2A est une variante qui est similaire à l'H2A conventionnelle; elle est codée par le gène H2AFY. Il existe trois isoformes de macroH2A : macroH2A1.1, macroH2A1.2 et macroH2A2 [8] qui semblent remplir des rôles distincts en fonction des tissus, du stade de développement ou des maladies (cancer) étudiés. Cette variante diffère de l'H2A canonique par l'ajout d'un domaine globulaire sur sa queue C-terminale. La MacroH2A est associée avec le chromosome X inactif dans les cellules femelles[9].
H2A.Bbd (corps de Barr-déficient) est spécifique aux mammifères[10].
Structure
H2A est composé d'un domaine globulaire et une longue queue N-terminale ou C-terminale à l'extrémité de la molécule. Le domaine terminaux sont les substrats des modifications post-traductionnelles de la protéine. Jusqu'à maintenant, il n'a été identifié aucune structure secondaire dans le domaine caudal. L'H2A dispose d'un repliement protéique appelé "repliement histone", qui est composé d'un domaine central de trois hélices qui sont reliés par deux boucles. Cette liaison est un " arrangement en poignée de main’. Il s'agit d'un motif hélice-tour-hélice, et permet la dimérisation avec l'histone H2B. Le repliement histone est conservé entre les variantes H2A au niveau structurel; mais la séquence génétique codant celui-ci varie selon les variantes[11].
La structure de la variante macroH2A a été obtenue par cristallographie aux rayons X, et présente un domaine globulaire (domaine macro : "macrodomain" en anglais ) en C-terminal. Le domaine conservé contient une structure de liaison à l'ADN et repliement peptidase[12]. La fonction de ce domaine macro n'est pas encore entièrement connue. Des recherches suggèrent que ce domaine conservé peut fonctionner comme un site d'ancrage, ou il peut aussi fonctionner comme enzyme modifiante. Récemment, il a été démontré que la variante macroH2A1.1 joue un rôle dans le métabolisme [13].
Fonction
Le repliement de l'ADN.- L'H2A est important dans l'empaquetage de l'ADN dans la chromatine. L'empaquetage affecte l'expression des gènes. L'H2A a été corrélée avec des modifications de l'ADN à l'épigénétique. L'H2A joue un rôle important dans la détermination de l'ensemble de la structure de la chromatine. Il a également été constaté que l'H2A régule l'expression des gènes[11].
La modification de l'ADN par H2A se produit dans le noyau de la cellule. Les protéines responsables de l'importation au cœur de la histones H2A sont les kariophérines et importines[14]. Des études récentes montrent également que la protéine 1 de l'assemblage du nucléosome est également utilisée pour le transport vers le noyau de l'H2A, de sorte qu'elle puisse se joindre à l'ADN. D'autres fonctions de l'H2A ont été associées à la variante H2A.Z. Cette variante est associée à l'activation de gènes, le silençage et la suppression de l'ARN antisens. En outre, l'H2A.Z a été utilisée dans des cellules humaines et des levures pour promouvoir le recrutement de l'ARN polymérase II[15].
Peptide antimicrobien.- Les histones sont des protéines cationiques eucaryotes conservées qui sont également impliquées dans les activités antimicrobiennes. Chez les vertébrés et les invertébrés, l'histone H2A est impliquée dans la réponse immunitaire de l'hôte pour agir comme peptide antimicrobien. Les H2A sont des molécules α-hélicoïdale, amphiphiles avec résidus hydrophobes et hydrophes aux côtés opposés qui augmentent son activité antimicrobienne[16].
Génétique
L'H2A est codée par de nombreux gènes dans le génome humain, y compris: H2AFB1, H2AFB2, H2AFB3, H2AFJ, H2AFV, H2AFX, H2AFY, H2AFY2 et H2AFZ. Les modèles génétiques entre les différentes molécules H2A sont essentiellement conservés parmi les variantes. Il existe une certaine variabilité dans l'expression des gènes entre la machine réglementrice qui contrôle l'expression de H2A. Des chercheurs ont étudié les lignées évolutives eucaryotes des histones et trouvé une diversification parmi les gènes régulateurs. Les différences les plus importantes ont été observées dans les motifs de séquence cis-régulatrices des gènes histone de l'octamère et les facteurs associés à des protéines. Une certaine variabilité dans la séquence des gènes fut observée entre les gènes des bactéries, des champignons, des plantes et des mammifères[11].
Une variante de la protéine H2A est H2ABbd (corps de Barr-déficient). Cette variante a une séquence génétique différente de celle de l'H2A[11]. D'autres variations liées à H2ABbd sont situés dans leur C-terminal. H2ABbd dispose d'un domaine C-terminal plus court que l'H2A. Les deux domaines C terminaux sont identiques à 48%. L'H2ABbd agit sur les chromosomes actifs. Elle est absente dans les chromosomes X inactifs (Xi) dans les fibroblastes. Elle est également associée avec l'H4 acétylée[17].
Les différentes fonctions de H2A.Z à l'égard des H2A classiques sont corrélées à leurs différences génétiques. Le gène H2A.Z est essentiel chez la levure, où il est appelé Htz1. En comparaison, les vertébrés ont deux gènes H2A.Z[11], appelés H2A.Z1 et H2A.Z2, qui donnent lieu à des protéines qui diffèrent en trois résidus. Au départ, les chercheurs ont pensé que ces gènes ont été redondants; cependant, lors de la création d'un mutant H2A.Z1, il fut observé une létalité chez les mammifères[17]. Par conséquent, H2A.Z1 est un gène ancestral. La fonction du variant H2A.Z2 n'a cependant pas encore été identifiée. On sait qu'il est transcrit chez les mammifères marins, et l'expression de ce gène est conservée chez les mammifères. Cette conservation suggère que ce gène est fonctionnel[17]. Chez les plantes, les protéines H2A.Z diffèrent pour certains résidus entre les espèces, et ces différences contribuent à la régulation du cycle cellulaire[17]. Ce phénomène a été observé uniquement chez les plantes.
Des arbres phylogénétiques ont été élaborés pour montrer les différences entre les variantes[18] - [19].
Modification de H2A
Les modifications que subit l'H2A sont actuellement sujet à investigation. Des sites de phosphorylation de la sérine ont été identifiés sur la structure de l'H2A. Il existe de grandes différences dans les modifications que subissent les différentes variantes de H2A. Par exemple, H2ABbd est dépourvue de résidus modifiés qui existent dans l'H2A classique[17]. Ces différentes modifications modifient la fonction de H2ABbd par rapport à H2A. La variante H2AX agit dans la réparation de l'ADN. Cette fonction dépend de la phosphorylation de l'extrémité C-terminale de H2AX[7], et uniquement lorsque H2AX est phosphorylée, peut celle-ci agir dans la réparation de l'ADN. La variante H2A.X diffère également de H2A au niveau des modifications post-traductionnelles. L'extrémité C-terminale de H2A.X contient un motif supplémentaire par rapport à H2A. Le motif qui est ajouté est Ser-Gln-(Glu/Asp)-(résidu hydrophobe)[17]. Ce motif est fortement phosphorylé au niveau du résidu sérine; lors de cette phopsphorylation H2A.X devient la variante yH2A.X. Cette phosphorylation se produit lors de cassures double-brin de l'ADN[17]. La modification des histones peut donc parfois entraîner un changement de fonction.
Notes et références
- Khorasanizadeh, « The nucleosome: From genomic organization to genomic regulation », Cell, vol. 116, no 2, , p. 259–72 (PMID 14744436)
- (en) David L. Nelson et Michael M. Cox, Lehninger principles of biochemistry, New York, W.H. Freeman, , 4th éd. (ISBN 0-7167-4339-6)
- Bosch et P Suau, « Changes in core histone variant composition in differentiating neurons: The roles of differential turnover and synthesis rates », European journal of cell biology, vol. 68, no 3, , p. 220–5 (PMID 8603674)
- Clemens Bönisch e Sandra B. Hake.
- Suto, M. J. Clarkson, D. J. Tremethick et K Luger, « Crystal structure of a nucleosome core particle containing the variant histone H2A.Z », Nature Structural Biology, vol. 7, no 12, , p. 1121–4 (PMID 11101893, DOI 10.1038/81971)
- Mizuguchi, X Shen, J Landry et W. H. Wu, « ATP-driven exchange of histone H2AZ variant catalyzed by SWR1 chromatin remodeling complex », Science, vol. 303, no 5656, , p. 343–8 (PMID 14645854, DOI 10.1126/science.1090701)
- Jakob, J Splinter, S Conrad et K. O. Voss, « DNA double-strand breaks in heterochromatin elicit fast repair protein recruitment, histone H2AX phosphorylation and relocation to euchromatin », Nucleic Acids Research, vol. 39, no 15, , p. 6489–99 (PMID 21511815, PMCID 3159438, DOI 10.1093/nar/gkr230)
- https://www.science.org/doi/10.1126/science.1529340?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
- Costanzi et J. R. Pehrson, « Histone macroH2A1 is concentrated in the inactive X chromosome of female mammals », Nature, vol. 393, no 6685, , p. 599–601 (PMID 9634239, DOI 10.1038/31275)
- Epigenie
- Mariño-Ramírez, I. K. Jordan et D Landsman, « Multiple independent evolutionary solutions to core histone gene regulation », Genome Biology, vol. 7, no 12, , R122 (PMID 17184543, PMCID 1794435, DOI 10.1186/gb-2006-7-12-r122)
- Allen, A. M. Buckle, S. C. Cordell et J Löwe, « The crystal structure of AF1521 a protein from Archaeoglobus fulgidus with homology to the non-histone domain of macroH2A », Journal of molecular biology, vol. 330, no 3, , p. 503–11 (PMID 12842467, DOI 10.1016/s0022-2836(03)00473-x)
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5791885/
- Mosammaparast, C. S. Ewart et L. F. Pemberton, « A role for nucleosome assembly protein 1 in the nuclear transport of histones H2A and H2B », The EMBO journal, vol. 21, no 23, , p. 6527–38 (PMID 12456659, PMCID 136951, DOI 10.1093/emboj/cdf647)
- Mariño-Ramírez, K. M. Levine, M Morales et S Zhang, « The Histone Database: An integrated resource for histones and histone fold-containing proteins », Database, vol. 2011, , bar048 (PMID 22025671, PMCID 3199919, DOI 10.1093/database/bar048)
- Jesu Arockiaraj, Annie J Gnanam, Venkatesh Kumaresan, Rajesh Palanisamy, Annie J Gnanam, Annie J Gnanam, Annie J Gnanam, Annie J Gnanam, Annie J Gnanam et Annie J Gnanam, « An unconventional antimicrobial protein histone from freshwater prawn Macrobrachium rosenbergii: Analysis of immune properties », Fish & Shellfish Immunology, vol. 35, no 5, , p. 1511–1522 (PMID 23994279, DOI 10.1016/j.fsi.2013.08.018)
- Talbert et S Henikoff, « Histone variants--ancient wrap artists of the epigenome », Nature Reviews Molecular Cell Biology, vol. 11, no 4, , p. 264–75 (PMID 20197778, DOI 10.1038/nrm2861)
- José M Eirín-López, Rodrigo González-Romero, Deanna Dryhurst, Toyotaka Ishibashi e Juan Ausió.
- Thomas H.Thatcher e Martin A.Gorovsky.