Glycogène
Le glycogène est un glucide complexe homopolymère du glucose. Il consiste en une chaîne de glucose lié en α (1-4) et est branché en α (1-6) tous les huit ou douze résidus. Il est utilisé par les animaux (et les champignons) comme réserve d'énergie chimique et permet de libérer rapidement du glucose (principalement dans le foie et dans les cellules musculaires) au même titre que l'amidon chez les végétaux. Les réserves en glycogène peuvent être rapidement mobilisées lors d'un soudain besoin en glucose, mais sont moins compactes que les réserves d'énergie sous forme de triglycérides dans le tissu adipeux.
| Glycogène | |
| |
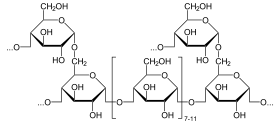
| Le glycogène est un polymère de glucose. | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.029.700 |
| No CE | 232-683-8 |
| PubChem | 439177 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche[1] |
| Propriétés chimiques | |
| Formule | (C6H10O5)n |
| Masse molaire | 106 à 107 g/mol |
| Propriétés physiques | |
| Solubilité | Soluble dans l'eau avec opalescence, insoluble dans l'alcool[1]. |
| Propriétés optiques | |
| Pouvoir rotatoire | [α]D25 +196 à +197°[1] |
| Précautions | |
| SIMDUT[2] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Historique
C'est à Claude Bernard qu'on doit d'abord l'idée de la fonction glycogénique du foie puis dans un deuxième temps l'isolement du glycogène. Cette découverte en 1856 marque une rupture importante avec les conceptions antérieures sur la nutrition. On pensait que seules les plantes pouvaient fabriquer les sucres, ensuite dégradés par les animaux dans un organe qui restait à déterminer, et dont Lavoisier pensait qu'il était le poumon. C'est en cherchant cet organe que Claude Bernard constata la présence de sucre à la sortie du foie (dans la veine sus-hépatique) et son absence à l'entrée (dans la veine porte). Chez des animaux nourris exclusivement de viande, la présence de sucre persistait à la sortie du foie. Les méthodes de dosage qu'il employait ne lui permettaient pas de retrouver le sucre au-dessous de 0,8 à 1 g/l, et donc dans la veine porte, ce qui le conduisit à donner une interprétation excessive de ses expériences. On crut longtemps qu'il s'était trompé, et que le foie ne faisait qu'emmagasiner le sucre sous forme de glycogène, avant de découvrir que la glycogénogenèse était bien le facteur essentiel de la formation du glycogène hépatique[3].
Chimie
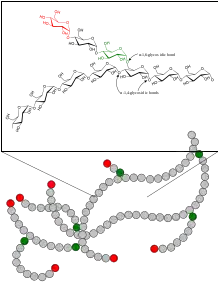
Le glycogène est une macromolécule de la famille des glucides constituée de nombreuses unités de D-glucose et qui constitue une réserve de glucose engrangée dans le foie et les muscles. C'est un polymère du glucose de structure arborescente, et de formule chimique (C6H10O5)n.
Chacune des chaînes latérales du glycogène comporte de dix à quinze unités de glucose, reliées entre elles par des liaisons α-(1-4). Les chaînes sont reliées entre elles par des liaisons α-(1-6). Le glycogène du foie contient ainsi trente mille unités de glucose.
Son poids moléculaire varie de 1 à 5 × 106 daltons (Da) selon son origine.
Biosynthèse
La glycogénogenèse se réalise en deux étapes. Dans un premier temps, grâce à la glycogène synthétase, a lieu la formation des chaînes linéaires à partir de l'amorce de deux à trois molécules de glucose qui se forment par le glycogénine, avec des liaisons osidiques de type alpha. Ensuite, l'enzyme branchante (α-1,4-D-glucanne)[4] relie entre elles les chaînes.
Rôle biologique
.tif.jpg.webp)
L'accumulation du glucose en glycogène est réalisé grâce à une enzyme : la glycogène synthase. C'est la glycogenèse.
Le foie réalise la glycogénolyse (hydrolyse du glycogène pour « reformer » du glucose à partir de ses réserves de glycogène) grâce à la glycogène phosphorylase. Si le glycogène vient à s'épuiser (au bout de douze heures de jeûne chez l'être humain), le foie utilise alors des protéines, du lactate (issus des muscles, entre autres) ou du glycérol (issu des lipides) pour reformer du glucose, par néoglucogenèse.
On trouve du glycogène également dans les muscles où il est entreposé puis dégradé en glucose lors des efforts musculaires. Contrairement au cas du foie, le glucose ainsi produit par la cellule musculaire n'est utilisé que par cette même cellule.
Contrôle hormonal de la synthèse et de la dégradation
La production de glycogène dans l'organisme est stimulée par l'insuline, hormone hypoglycémiante. Par la fixation à son récepteur de la famille tyrosine kinase, l'insuline active une cascade de signalisations intracellulaires aboutissant à l'activation de la glycogène synthase. La dégradation du glycogène en glucose est stimulée par le glucagon et l'adrénaline et est assurée majoritairement par une glucosidase de type amylase ainsi qu'une glycogène phosphorylase. Les deux hormones hyperglycémiantes se fixent sur des récepteurs à sept domaines transmembranaires couplés à des protéines G qui activent l'adénylate cyclase qui augmente le taux d'AMP cyclique dans la cellule, ce qui active une protéine kinase A qui inhibe la glycogène synthase et qui active la glycogène phosphorylase.
Maladies liées à des déficits enzymatiques
Les déficits en enzymes intervenant dans le métabolisme du glycogène donnent lieu à des maladies neuromusculaires rares appelées « glycogénoses ».
- Glycogénose de type 0 : déficit en glycogène synthétase[5].
- Glycogénose de type I : résulte de l'absence de glucose-6-phosphatase[6].
- Glycogénose de type II ou maladie de Pompe : absence d'α(1→4) glucocidase[5] - [6].
- Glycogénose de type III ou maladie de Forbes : absence d'α(1→6) glucocidase[5] - [6].
- Glycogénose de type IV ou maladie d'Andersen : absence de glucosyl (1→4)-(1→6) (glycosyltransférase)[5] - [6].
- Glycogénose de type V ou maladie de Mc Ardle : déficit en phorphorylase musculaire[6] - [5].
- Glycogénose de type VIb ou maladie de Hers : déficit en phorphorylase hépatique[6] - [5].
- Glycogénose de type VII ou maladie de Tarui : déficit en phosphofructokinase musculaire[5].
- Glycogénose de type VIa, VIII et IX : déficit en phosphorylase kinase[7].
- Glycogénose de type X ou maladie de Di Mauro : déficit en phosphoglycérate mutase[5].
- Glycogénose de type XIV : déficit en glycogène synthase musculaire[5].
Notes et références
- The Merck Index, 13e éd., 4509.
- « Glycogène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- Mirko Drazen Grmek, Le legs de Claude Bernard, 1997, 440 p.
- E.C.2.4.1.18.
- Information bibliographique sur les maladies neuromusculaires rares, sur myobase.org.
- P. Louisot, Biochimie, Éd. SIMEP, 1983, p. 107.
- Information bibliographique sur les maladies neuromusculaires rares - déficit en phosphorylase kinase, sur myobase.org.
Voir aussi
Articles connexes
Bibliographie
- Drochmans P., Morphologie du glycogène : Étude au microscope électronique de colorations négatives du glycogène particulaire, Journal of Ultrastructure Research, 1962, 6(2), 141-163 (résumé).