Catalyse acide ou basique
Une catalyse acide ou une catalyse basique est la catalyse d'une réaction chimique par un acide ou une base. Dans ces réactions, l'acide est souvent un ion hydronium (« proton ») et la base un ion hydroxyde. On peut citer parmi les réactions typiquement catalysées par transfert de proton les estérifications et les aldolisations. Dans ces réactions, l'acide conjugué du groupe carbonyle est un meilleur électrophile que le groupe carbonyle en lui-même.
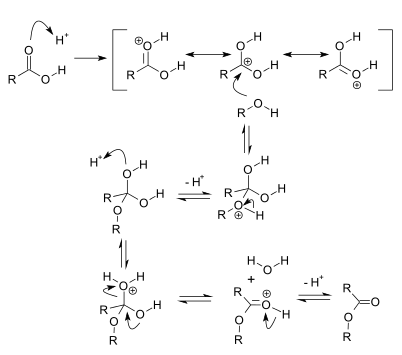
Ces catalyses peuvent être de deux types : catalyse spécifique et catalyse générale.
Cinétique
Catalyse spécifique
En catalyse acide spécifique dans un solvant S, la vitesse de réaction est proportionnelle à la concentration en molécules de solvant protonées SH+[1]. L'acide catalyseur (AH) ne contribue en lui-même qu'à accélérer la réaction en déplaçant l'équilibre chimique entre les formes S, AH et SH+, favorisant cette dernière.
- S + AH → SH+ + A−
Par exemple en solution aqueuse tamponnée, la vitesse de réaction pour un réactif R1 dépend du pH du système mais pas de la concentration des différents acides :
Ce type de cinétique chimique est observé quand un réactif R1 est rapidement en équilibre avec sa forme protonée R1H+ qui réagit ensuite lentement pour donner R2, le produit de réaction. C'est par exemple le cas d'une aldolisation catalysée par un acide.
Catalyse générale
En catalyse acide générale, toutes les espèces capables de donner des protons contribuent à l'accélération de la vitesse de réaction[2]. Les acides les plus forts sont les plus efficaces. Les réactions dans lesquelles le transfert de proton est déterminant pour la vitesse de réaction montrent une forme de catalyse générale, comme par exemple les réactions de couplage azo.
Le fait de changer la vitesse de réaction en changeant la concentration en tampon tout en maintenant le pH constant est un indice d'une cinétique de type catalyse générale. Au contraire, une vitesse constante dans ces conditions indique une catalyse acide spécifique.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Acid catalysis » (voir la liste des auteurs).
- (en) « Specofic acid catalysis », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
- (en) « General acid catalysis », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
![{\displaystyle v=-{\frac {\mathrm {d} [R_{1}]}{\mathrm {d} t}}=k[SH^{+}][R_{1}][R_{2}]}](https://img.franco.wiki/i/ba9f231ccfec4adf4326ceb2b79781d9f44f67ed.svg)
![{\displaystyle v=-{\frac {\mathrm {d} [R_{1}]}{\mathrm {d} t}}=k_{1}[SH^{+}][R_{1}][R_{2}]+k_{2}[AH^{1}][R_{1}][R_{2}]+k_{3}[AH^{2}][R_{1}][R_{2}]+...}](https://img.franco.wiki/i/6ceb108c5d512c921750fe01d4d2a50cf1c17860.svg)