Acétate
Un acétate ou éthanoate (IUPAC) est un sel ou un ester de l'acide acétique. La formule de l'ion acétate est CH3COO−.
| Ion acétate | |
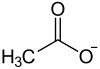
| |
| Identification | |
|---|---|
| Synonymes |
éthanoate, |
| No CAS | |
| PubChem | 175 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C2H3O2- |
| Masse molaire[1] | 59,044 ± 0,002 4 g/mol C 40,68 %, H 5,12 %, O 54,19 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Le terme acétate peut aussi faire référence à l’acétate de cellulose, en particulier les fibres mais également (au Québec), à d'autres produits dérivés tels que les transparents pour rétroprojecteurs ou les disques acétate utilisés pour les enregistrements audio. L’acétate a connu de nombreux usages, civils, militaires et est encore utilisé dans de nombreux produits d’entretien.
Le mot « acétate » vient du latin « acetum », signifiant « vinaigre »[2].
Notation
L’abréviation Ac ou AC est parfois utilisée dans les formules chimiques pour indiquer l’ion acétate.
Par exemple la formule de l’acétate de sodium pouvait s’écrire NaAc, au lieu des formules plus modernes CH3COONa ou NaC2H3O2. Dans le domaine de la chimie organique, l’abréviation Ac fait référence au groupe acétyle CH3CO, l’acétate y est donc désigné sous la forme −OAc, l’acétate de sodium est écrit NaOAc et l'acétate d’éthyle EtOAc.
Dérivés
Esters
Les acétates peuvent être des esters de l'acide acétique. C'est le cas de :
Sels
Les acétates peuvent être des sels de l'acide acétique. C'est le cas de :
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Pierre de Menten, Dictionnaire de chimie : Une approche étymologique et historique, De Boeck, , 395 p. (ISBN 978-2-8041-8175-8, lire en ligne), p.17