Sulfonium
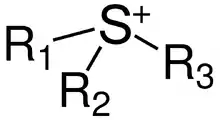
Un ion sulfonium (parfois sulphonium ou sulfanium) est un cation constitué d'un atome de soufre comportant trois substituants organiques. Les ions sulfonium ont pour formule générale [SR3]+. Avec un contre-anion, ils forment les sels de sulfonium.
Occurrence
On trouve des sulfonium, ou pour être plus précis des méthioniniums, comme la S-adénosylméthionine assez couramment dans la nature, où elle sert de radical adénosoyle. Ce radical participe à la biosynthèse de nombreux composés[1].
Un autre sulfonium (méthioninium) présent dans la nature est la S-méthylméthionine.
Structure
Les composés sulfonium ont une géométrie pyramidale au niveau de l'atome de soufre. Ainsi, le cation triméthylsulfonium (Me3S+) est structurellement similaire au composé isoélectronique triméthylphosphine. Les composés sulfonium où les trois substiaunt sont différents sont chiraux et optiquement stables[2].
Synthèse
Les composés sulfonium sont en général synthétisés par réaction entre un thioéther et un halogénoalcane. Par exemple, la réaction entre le sulfure de diméthyle et l'iodométhane produit l'iodure de triméthylsulfonium :
- CH3–S–CH3 + CH3–I → (CH3)3S+ + I−
Avant la réaction, l'atome de soufre possède de doublets non-liants ; l'un de ces doublets se lie au groupe méthyle de l'iodométhane. Au même moment, dans un mécanisme de substitution nucléophile bimoléculaire (SN2), le groupe iodure nucléofuge part. le résultat est une cation (positivement chargé) triméthylsulfonium, dont la charge est équilibrée par son contre-anion iodure. La réaction est rapide, et l'est encore plus avec des agents méthylants forts, tele que le trifluorométhanesulfonate de méthyle.
Applications
Synthèse organique
Les centres de sulfonium servent à stabiliser la formation d'ylures, composés utiles dans les réactions de formation de liaison C-C[3].
Industrie
Certains colorants azo sont modifiés avec des groupes sulfonium pour leur donner une charge positive. Le composé triflate de triphénylsulfonium est un photoacide, un composé qui se convertit en acide sous l'action de la lumière.
Notes et références
- Layer, G.; Heinz, D. W.; Jahn, D.; Schubert, W.-D. "Structure and function of radical SAM enzymes" Current Opinion in Chemical Biology 2004, volume 8, 468-476. DOI 10.1016/j.cbpa.2004.08.001
- March, J. “Advanced Organic Chemistry” 5th Ed. J. Wiley and Sons, 1992: New York. (ISBN 0-471-60180-2).
- Mitchell J. Bogdanowicz, Barry M. Trost, Cyclopropylphenylsulfonium Tetrafluoroborate, Org. Synth., coll. « vol. 6 », , p. 364
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Sulfonium » (voir la liste des auteurs).
Voir aussi
- Sulfure R-S-R
- Sulfate R-SO4-R
- Sulfite R-SO3-R
- Sulfonate R-SO3−
- Composé onium