Pentasulfure de titanocène
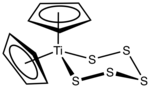
Le pentasulfure de titanocène est un métallocène organotitane de formule chimique Cp2TiS5, où Cp représente un ligand cyclopentadiényle C5H5. Il s'agit d'un solide rouge vif soluble dans les solvants organiques. Il fait l'objet de recherches pour produire des allotropes peu courants du soufre ainsi que certains composés cycliques apparentés.
| Pentasulfure de titanocène | |
| |
| Structure du pentasulfure de titanocène | |
| Identification | |
|---|---|
| No CAS | |
| PubChem | 92000650 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H10S5Ti |
| Masse molaire[1] | 338,378 ± 0,035 g/mol C 35,5 %, H 2,98 %, S 47,38 %, Ti 14,15 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
On l'obtient en traitant du dichlorure de titanocène Cp2TiCl2 avec des sels de polysulfures[2]. Il avait été préparé pour la première fois par addition de soufre élémentaire à du dicarbonyle de titanocène (C5H5)2Ti(CO)2[3] :
- (η5-C5H5)2Ti(CO)2 + 58 S8 ⟶ (η5-C5H5)2TiS5 + 2 CO.
Il est considéré comme complexe pseudotétraédrique du titane(IV). Les liaisons Ti–S ont une longueur de 242,0 et 244,6 pm tandis que les liaisons S–S ont une longueur normale de 205,1 à 205,9 pm[4]. Le spectre RMN du pentasulfure de titanocène est celui d'une molécule fluxionnelle (en) en raison de l'équilibre chaise-chaise du cycle TiS5 qui donne un signal équivalent à celui du cyclopentadiényle à température élevée[5]. Ce complexe réagit avec les chlorures de soufre et de selenium ExCl2 pour donner du dichlorure de titanocène Cp2TiCl2 et cycles S5+x et S5Sex. Ceci est illustré par la synthèse du cycloheptasoufre S7 à partir du dichlorure de disoufre S2Cl2[6] :
- (η5-C5H5)2TiS5 + S2Cl2 ⟶ (η5-C5H5)2TiCl2 + S7.
Il a ainsi été possible d'obtenir les allotropes cyclo-Sn, où n = 9 à 15, 18 et 20, avec des dichlorosulfanes de longueur convenable Sn-5Cl2[7] :
- (η5-C5H5)2TiS5 + Sn−5Cl2 ⟶ cyclo-Sn + (η5-C5H5)2TiCl2.
Le pentasulfure de titanocène réagit avec les alcènes et les cétènes pour donner des hétérocycles contenant du titane, du carbone et du soufre. Avec les trialkylphosphines, le cycle dimérise en cycles de diverses tailles selon la trialkylphosphine utilisée[8].
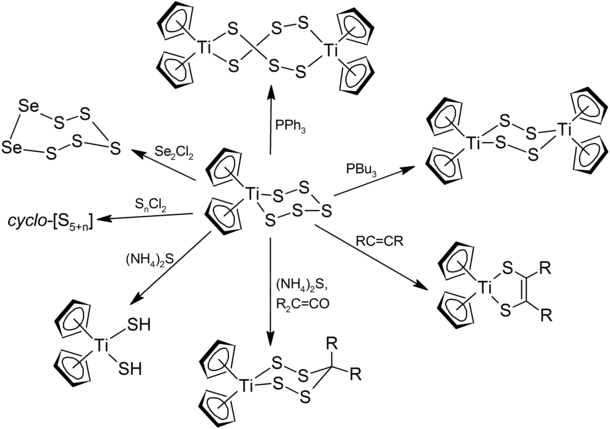
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Alan Shaver, James M. Mccall, Gabriela Marmolejo, F. Bottomley, E. C. Ferris et J. A. Gladysz, « Cyclometallapolysulfanes (and Selanes) of Bis(η5-Cyclopentadienyl) Titanium(IV), Zirconium(IV), Molybdenum(IV), and Tungsten(IV) », Inorganic Syntheses, vol. 27, (DOI 10.1002/9780470132586.ch11, lire en ligne)
- (en) « π-Complexes of Group IVA metals with cyclopentadiene, indene, and fluorine », Bulletin de la société chimique de France, vol. 11, , p. 3548-3564.
- (en) Earl F. Epstein et Ivan Bernal, « Pentachalcogenide dianions in transition-metal complexes: crystal structure of bis-(π-cyclopentadienyl)titanium pentasulphide », Journal of the Chemical Society D: Chemical Communications, vol. 1970, no 7, , p. 410-411 (DOI 10.1039/C29700000410, lire en ligne)
- (en) Alan Shaver et James M. McCall, « Preparation and variable-temperature NMR studies of the metallocyclosulfanes Cp2MS5 and (Me5Cp)2MS3, where M = Ti, Zr and Hf », Organometallics, vol. 3, no 12, , p. 1823-1829 (DOI 10.1021/om00090a008, lire en ligne)
- (en) Ralf Steudel et Bodo Eckert, « Solid Sulfur Allotropes. Elemental Sulfur and Sulfur-Rich Compounds I », Topics in Current Chemistry, vol. 230, , p. 1-80 (DOI 10.1007/b12110, lire en ligne)
- (en) N. N. Greenwood et A. Earnshaw, Chemistry of the Elements, 2e éd., Butterworth-Heinemann, 1997, p. 657. (ISBN 978-0-08-037941-8)
- (en) F. Albert Cotton, Geoffrey Wilkinson, Carlos A. Murillo et Manfred Bochmann, Advanced Inorganic Chemistry, 6e éd., Wiley, 1999. (ISBN 978-0471199571).