Hyperplasie nodulaire focale
L'hyperplasie nodulaire focale (HNF) est une tumeur bénigne du foie principalement observée chez la femme. Généralement asymptomatique et ne nécessitant que rarement un traitement chirurgical, son diagnostic fait habituellement appel à l'association de diverses modalités d'imagerie.
Anatomopathologie
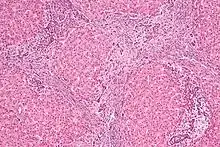
L’hyperplasie nodulaire focale est une tumeur bénigne[1] - [2] de nature hépatocytaire[2] dont le diagnostic anatomopathologique est simple[3].
Sur le plan physiopathologique, la survenue de l'HNF semble liée à une perturbation locale primitive du flux sanguin (possiblement en rapport avec une malformation artério-veineuse[4]) à l'origine secondairement d'une réaction hyperplasique[5] - [6]. Ce phénomène est à rapprocher de la survenue d'hyperplasie nodulaire régénérative en présence d'autres anomalies vasculaires telles que l'hypertension portale ou le syndrome de Budd-Chiari[3].
Parfois rapprochée histologiquement d'une forme focale de cirrhose[5] - [7], l'hyperplasie nodulaire focale est formée d'hépatocytes organisés en travées. Ces travées sont séparées par des cloisons fibreuses[1] émanant d'une cicatrice centrale[2]. Cette dernière est d'autant plus fréquemment visible que la tumeur est volumineuse[1]. La cicatrice est de nature fibreuse et contient également des éléments vasculaires (qui se distribuent ensuite de façon radiaire dans les cloisons)[2].
La lésion possède un système de drainage biliaire anormal [4] - [6] avec en particulier une absence de canalicules biliaires[1] à l'origine d'un ralentissement de l'excrétion biliaire[6]. Il existe en revanche une prolifération cholangiolaire au contact des cloisons fibreuses[1] - [2]. Comme dans le parenchyme hépatique sain, on retrouve également des cellules de Kupffer au sein de l'HNF[8].
La vascularisation artérielle provient de l'artère hépatique. Le sang artériel gagne l'artère centrale de la lésion avant de se propager de façon radiaire dans l'ensemble de la lésion par des artérioles situées dans les cloisons fibreuses. Le drainage veineux est périphérique et s'effectue par le biais des veines hépatiques. Il n'y a donc pas de participation de la vascularisation portale[4].
Macroscopiquement il s'agit d'une lésion bien limitée mais non encapsulée[1] - [2]. Elle est de forme arrondie et souvent lobulée[1] - [2]. La taille de la lésion est très variable mais est en général inférieure à 5 cm[6]. En dehors de la cicatrice centrale, l'HNF est une lésion homogène généralement dépourvue de plage hémorragique, nécrotique ou encore de calcification[6].
Épidémiologie
La prévalence de l'HNF dans la population générale est estimée entre 0,03 %[3] et 0,9 %[1], ce qui en fait la troisième tumeur hépatique la plus fréquente derrière le kyste biliaire et l'hémangiome[6] - [1], et donc la deuxième tumeur hépatique non vasculaire la plus fréquente[5].
L'HNF survient préférentiellement chez la femme [5] - [3] avec un sex ratio aux alentours de 8 pour 1[2] - [1] - [6] ce qui suggère une influence hormonale. La tumeur exprimerait des récepteurs aux œstrogènes [7] mais le rôle de ces composés dans la croissance de l'HNF est très discuté avec des résultats contradictoires[7]. La contraception orale a longtemps été accusée de favoriser la croissance en taille des lésions[2] - [4] mais cette hypothèse semble aujourd'hui réfutée[2] - [1].
L'âge moyen de découverte est d'environ 40 ans, un peu plus tardif chez l'homme[2] - [1]. De rares cas pédiatriques ont toutefois été rapportés (environ 200 cas dans la littérature), y compris en période néonatale[9].
Enfin le tabagisme serait un facteur de risque de survenue d'HNF[10].
L'hyperplasie nodulaire focale peut survenir de façon isolée, multiple ou encore associée à d'autres lésions bénignes (hémangiome, adénome)[4] - [2] - [6]. La multiplicité des HNF est également corrélée à la survenue de tumeurs cérébrales : méningiome et astrocytome[6].
Clinique
La lésion est dans la grande majorité des cas asymptomatique[3] - [5]. Sa découverte est donc le plus souvent fortuite lors du bilan de douleurs abdominales ou encore de perturbations du bilan biologique hépatique[1] - [3].
En cas de lésion de grande taille, l'effet de masse exercé peut être à l'origine d'une douleur abdominale ainsi que d'une hépatomégalie clinique[6].
Chez l'enfant l'HNF est plus fréquemment symptomatique que chez l'adulte avec des douleurs abdominales au premier plan[9].
Des complications à type de rupture et d'hémorragie ont toutefois été décrites[4] - [11].
Imagerie
Échographie

L’échographie est un examen souvent à l’origine de la découverte fortuite de l’hyperplasie nodulaire focale[3].
L’hyperplasie nodulaire focale apparaît généralement isoéchogène, parfois discrètement hypoéchogène, au parenchyme adjacent[1] - [3] - [12]. Ce faible contraste entre la lésion et son environnement la rend difficile à détecter[8]. L'effet de masse exercé par la lésion sur les vaisseaux avoisinants peut être une aide au repérage de l'HNF[1]. À noter qu'en cas de stéatose hépatique, l'HNF apparaît hypoéchogène[12] compte tenu d'une élévation de l'échogénicité du foie.
L'HNF est une lésion homogène, la cicatrice centrale étant visible dans seulement un cas sur cinq[12]. Les contours de la lésion sont nets et lobulés[12].
Lorsqu’elle est visible, la cicatrice centrale est hyperéchogène[1] - [3] - [12] (mais possiblement hypoéchogène [6]). L’étude en Doppler couleur permet de visualiser au centre de la lésion une hypervascularisation traduisant la présence de l’artère afférente[12].
L’étude en Doppler pulsé met en évidence des vitesses systoliques élevées[6] - [12] et un index de résistance d’environ 0,5[1] - [3].
L’élastographie peut être utile pour différencier l’HNF des autres lésions bénignes. Celle-ci est en effet la plus dure des lésions hépatiques bénignes [12]. Son module d’élasticité moyen est de 47 kPa contre 12 kPa pour l’adénome hépatocellulaire[13].
L’échographie de contraste en revanche est un examen présentant une très bonne sensibilité et une bonne spécificité dans le diagnostic d’hyperplasie nodulaire focale[1]. Le rehaussement lésionnel est intense à la phase artérielle[1] avec un remplissage typiquement centrifuge présentant un aspect radiaire[1]. La lésion ne présente pas de lavage et reste donc en hypersignal (plus ou moins marqué) par rapport au parenchyme adjacent[8].
Scanner
L’acquisition doit être réalisée sans injection, puis aux phases artérielle, portale et tardive d’une injection intraveineuse de produit de contraste iodé[1].
Spontanément l’hyperplasie nodulaire focale est isodense voire légèrement hypodense par rapport au parenchyme adjacent[1] - [6]. Il existe une hypervascularisation intense au temps artériel[1] - [6] avec rehaussement supérieur à celui de l’adénome[1]. On assiste ensuite à un retour à l'isodensité aux temps ultérieurs[3].
La cicatrice centrale est surtout visible en cas de lésion volumineuse[1]. Son rehaussement est plus tardif que celui du reste de la lésion. Elle apparaît donc hypovasculaire au temps artériel[1] et hyperdense au temps tardif[6].
IRM
Spontanément, l’hyperplasie nodulaire focale est peu discernable du parenchyme adjacent[1]. Elle apparaît ainsi en isosignal T1 (ou discret hyposignal T1) et en isosignal T2 (ou discret hypersignal T2)[1] - [2] - [6]. La cicatrice centrale est-elle en hyposignal T1 et franc hypersignal T2[1] - [2] - [6]. Cet hypersignal T2 s’explique par la prolifération cholangiolaire[1].
La cinétique de rehaussement après injection de produit de contraste est identique à celle observée en scanner ou encore en échographie de contraste. On met en évidence un hypersignal intense au temps artériel avec un retour à l’isosignal au temps portal[1] - [2] - [6]. La prise de contraste de la cicatrice centrale est retardée, surtout visible au temps tardif[2] - [6].
L’utilisation d’un produit de contraste hépato-spécifique (par exemple le gadobénate de diméglumine) est utile pour le diagnostic différentiel notamment par rapport à l’adénome hépatocellulaire[1] en mettant en évidence un hypersignal lésionnel tardif (1h après l’injection)[2]. Cet hypersignal est en rapport avec les malformations du système de drainage biliaire[6] ralentissant l’excrétion de la bile.
Les séquences de diffusion peuvent être utiles pour la détection de l’HNF qui apparaît en hypersignal sur les séquences à b élevé[1]. Le calcul de l’ADC n’apporte pas de renseignement utile pour la caractérisation de la lésion ou pour la détection (valeur moyenne d’ADC très proche de celle du parenchyme hépatique normal : 1,6 × 10−3 mm2/s)[1] - [14]. L’IRM de perfusion pourrait apporter des résultats intéressants, l’HNF s’y distinguant du parenchyme adjacent[14].
Autres modalités
La présence intra-lésionnelle de cellules de Küppfer explique la mise en évidence fréquente d’une hyperfixation à la scintigraphie au soufre colloïdal marqué au 99 m-Tc. Cette particularité est utile au diagnostic différentiel (adénome hépatique, carcinome hépatocellulaire et métastases)[4] - [6].
Diagnostics différentiels
Le principal diagnostic différentiel de l'hyperplasie nodulaire focale en imagerie est l'adénome hépatocellulaire[6] - [2]. Généralement, ce dernier apparaît plus hétérogène, sans cicatrice centrale et ne retient pas le produit de contraste hépatopécifique à la phase d'élimination biliaire[6]. Toutefois il est parfois impossible de trancher entre l'une ou l'autre de ces tumeurs hépatocytaires[2].
Parmi les autres diagnostics différentiels on retrouve l'hémangiome, le carcinome hépatocellulaire (en particulier fibrolamellaire) ainsi que les métastases hypervasculaires[6] - [2].
La ponction-biopsie hépatique peut fournir une aide supplémentaire[1] - [2] et apparaît plus rentable si elle est réalisée dans la zone de la cicatrice centrale[1].
Prise en charge
Une fois le diagnostic posé, la surveillance n’est pas nécessaire[1].
Un traitement chirurgical peut être proposé en cas de lésion symptomatique[6].
Références
- Valérie Vilgrain et Denis Régent, Imagerie de l'abdomen, Paris, Médecine sciences publications-[Lavoisier], , 1056 p. (ISBN 978-2-257-20417-2, lire en ligne)
- Christophe Aubé, IRM du foie et des voies biliaires, Montpellier, Sauramps médical, , 277 p. (ISBN 978-2-84023-695-5, lire en ligne)
- C. Laurent, H. Trillaud, P. Bioulac-Sage et C. Balabaud, « Hyperplasie nodulaire focale », EMC - Hépatologie, vol. 1, no 3, , p. 107 - 112 (lire en ligne)
- (en) « Focal nodular hyperplasia », sur Radiopaedia (consulté le )
- Lucas Maillette de Buy Wenniger, Valeska Terpstra et Ulrich Beuers, « Focal nodular hyperplasia and hepatic adenoma: epidemiology and pathology », Digestive Surgery, vol. 27, no 1, , p. 24–31 (ISSN 1421-9883, PMID 20357448, DOI 10.1159/000268404, lire en ligne, consulté le )
- Michael P. Federle, Diagnostic Imaging : Abdomen, Amirsys, , 992 p. (ISBN 978-1-4160-2541-2, lire en ligne)
- Manju D Chandrasegaram, Ali Shah, John W Chen et Andrew Ruszkiewicz, « Oestrogen hormone receptors in focal nodular hyperplasia », HPB : The Official Journal of the International Hepato Pancreato Biliary Association, vol. 17, no 6, , p. 502–507 (ISSN 1365-182X, PMID 25728618, PMCID PMC4430780, DOI 10.1111/hpb.12387, lire en ligne, consulté le )
- Francois Tranquart, Échographie de contraste : Méthodologie et Applications cliniques, Paris, Springer-Verlag Paris, 328 p. (ISBN 978-2-287-33294-4)
- Stéphanie Franchi-Abella et Sophie Branchereau, « Benign Hepatocellular Tumors in Children: Focal Nodular Hyperplasia and Hepatocellular Adenoma », International Journal of Hepatology, vol. 2013, (ISSN 2090-3448, PMID 23555058, PMCID PMC3608344, DOI 10.1155/2013/215064, lire en ligne, consulté le )
- Astrid Scalori, Alessandra Tavani, Silvano Gallus et Carlo La Vecchia, « Risk factors for focal nodular hyperplasia of the liver: an Italian case-control study », The American Journal of Gastroenterology, vol. 97, no 9, , p. 2371–2373 (ISSN 0002-9270, PMID 12358258, DOI 10.1111/j.1572-0241.2002.05796.x, lire en ligne, consulté le )
- « Rupture d'une hyperplasie nodulaire focale. À propos de deux cas », Annales de Chirurgie, vol. 131, , p. 279 - 282 (lire en ligne).
- Olivier Lucidarme, Echographie abdominale, Elsevier Health Sciences France, , 480 p. (ISBN 978-2-294-74360-3, lire en ligne)
- Thomas Brunel, Aymeric Guibal, Camille Boularan et Christian Ducerf, « Focal nodular hyperplasia and hepatocellular adenoma: The value of shear wave elastography for differential diagnosis », European Journal of Radiology, vol. 84, no 11, , p. 2059–2064 (ISSN 1872-7727, PMID 26299323, DOI 10.1016/j.ejrad.2015.07.029, lire en ligne, consulté le )
- Francescamaria Donati, Piero Boraschi, Roberto Gigoni et Simonetta Salemi, « Focal nodular hyperplasia of the liver: diffusion and perfusion MRI characteristics », Magnetic Resonance Imaging, vol. 31, no 1, , p. 10–16 (ISSN 1873-5894, PMID 22898696, DOI 10.1016/j.mri.2012.06.031, lire en ligne, consulté le )