Hydrosulfure d'ammonium
L'hydrosulfure d'ammonium ou hydrogénosulfure d'ammonium ou bisulfure d'ammonium, est le composé chimique de formule NH4SH. Il s'agit d'un sel de cations ammonium NH4+ et d'anions hydrosulfure SH− se présentant généralement en solution aqueuse fumante de couleur jaune-orangé, plus rarement sous forme de cristaux incolores. On l'obtient en mélangeant du sulfure d'hydrogène H2S avec de l'ammoniac NH3.
| Hydrosulfure d'ammonium | |
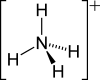 Structure de l'hydrosulfure d'ammonium |
|
| Identification | |
|---|---|
| Nom UICPA | hydrosulfure d'ammonium |
| Synonymes |
hydrogénosulfure d'ammonium |
| No CAS | |
| No ECHA | 100.031.974 |
| No CE | 235-184-3 |
| PubChem | |
| InChI | |
| Apparence | cristaux incolores |
| Propriétés chimiques | |
| Formule | [NH4+][HS−] |
| Masse molaire[1] | 51,111 ± 0,006 g/mol H 9,86 %, N 27,4 %, S 62,74 %, |
| Propriétés physiques | |
| Solubilité | soluble dans l'eau en toutes proportions |
| Masse volumique | 1 170 kg/m3 |
| Unités du SI et CNTP, sauf indication contraire. | |
Préparation
De l'hydrosulfure d'ammonium peut être produit en faisant barboter du sulfure d'hydrogène dans une solution d'ammoniac concentrée[2]. La réaction se produit à température ambiante et conduit à l'espèce chimique (NH4)2S·2NH4HS, qui donne (NH4)2S·12NH4HS après refroidissement à 0 °C[3]. En poursuivant le passage du sulfure d'hydrogène dans ce composé à 0 °C, on obtient l'hydrosulfure d'ammonium NH4SH.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Goodman, J. T.; Rauchfuss, T. B.,, « Tetraethylammonium-tetrathioperrhenate [Et4N][ReS4] », Inorganic Syntheses, vol. 33, , p. 107–110
- (en) W. P. Bloxam, « The Sulphides and Polysulphides of Ammonium », J. Chem. Soc., Trans., vol. 67, , p. 283 (DOI 10.1039/CT8956700277)