Couplage de Glaser
Le couplage de Glaser est une réaction de couplage d'alcynes en présence de dioxygène, d'une base et de sel de cuivre(I)[1] - [2] ou cuivre(II)[1] menant à la formation de diynes symétriques.
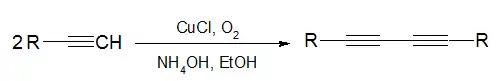
Cette réaction tient son nom de Carl Andreas Glaser (de) qui l'a découverte en 1869[3] - [4].
Mécanisme
Le mécanisme exact est méconnu et encore sujet à débat[1]. Il a été montré que le mécanisme radicalaire initialement proposé est inexact.
Modifications
Les conditions originelles de Glaser utilisent de l'ammoniaque ou de la pyridine comme base et du chlorure de cuivre(I). Ces conditions sont tombées en désuétude en 1962 au profit de celles de Hay, qui utilisent de la TMEDA et une amine tertiaire[2].
Couplage d'Eglinton
Dans cette réaction, décrite pour la première fois en 1956, le cuivre est au degré d'oxydation +II et joue le rôle de l'oxydant[2].
Voir aussi
Notes et références
- (en) László Kürti et Barbara Czakó, Strategic Applications of Named Reactions in Organic Synthesis : Background and Detailed Mechanisms, Amsterdam, Elsevier Academic press, , 758 p. (ISBN 0-12-429785-4), p. 186
- Jacques Drouin, Introduction à la chimie organique : Les molécules organiques dans votre environnement. Usages, toxicité, synthèse et réactivité, Corbas, Librairie du Cèdre, , 1re éd., 785 p. (ISBN 978-2-916346-00-7 et 2-916346-00-7), p. 279
- (de) C. Glaser, « Untersuchungen über einige Derivate der Zimmtsäure », Liebigs Ann. Chem., vol. 154, no 2, , p. 137–171 (ISSN 0075-4617, DOI 10.1002/jlac.18701540202).
- (de) C. Glaser, « Beiträge zur Kenntniss des Acetenylbenzols », Ber. Dtsch. Chem. Ges., vol. 2, no 1, , p. 422–424 (ISSN 0365-9496, DOI 10.1002/cber.186900201183, lire en ligne).