Aurure de césium
L'aurure de césium est un composé ionique de formule chimique CsAu contenant l'anion aurure Au−, le césium étant l'un des rares éléments susceptibles d'amener l'or à un état d'oxydation négatif[2]. Il a été observé pour la première fois par Joseph Lagowski (en) en 1978[3]. On l'obtient en chauffant un mélange stœchiométrique de césium et d'or : les deux liquides de couleur dorée réagissent pour former un produit clair. La solution dans l'ammoniac liquide est brune, l'adduit avec l'ammonium NH4+ est bleu foncé, tandis que le solide est jaune, couleur des deux métaux formant le composé.
| Aurure de césium | |
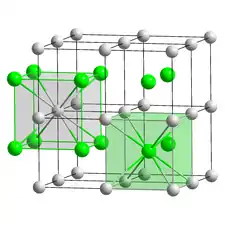
| |
| __ Cs+ __ Au− | |
| Identification | |
|---|---|
| Nom UICPA | aurure de césium |
| Propriétés chimiques | |
| Formule | CsAu |
| Masse molaire[1] | 329,872 021 ± 4,0E−6 g/mol Au 59,71 %, Cs 40,29 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Bien qu'il s'agisse d'un composé de deux métaux, l'aurure de césium n'est pas un métal car les électrons des deux métaux sont engagés dans les liaisons ioniques.
Ce composé réagit violemment avec l'eau, donnant de l'hydroxyde de césium CsOH, de l'or métallique Au et de l'hydrogène H2. Dans l'ammoniac liquide, on peut le faire réagir avec une résine échangeuse d'ions spécifique au césium pour former de l'aurure de tétraméthylammonium[4] [(H3C)4N]Au.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Guochun Yang, Yanchao Wang, Feng Peng, Aitor Bergara et Yanming Ma, « Gold as a 6p-Element in Dense Lithium Aurides », Journal of the American Chemical Society, vol. 138, no 12, , p. 4046-4052 (PMID 26942558, DOI 10.1021/jacs.5b11768, lire en ligne)
- (en) William J. Peer et J. J. Lagowski, « Metal-ammonia solutions. 11. Gold(1-), a solvated transition metal anion », Journal of the American Chemical Society, vol. 100, no 19, , p. 6260-6261 (DOI 10.1021/ja00487a064, lire en ligne)
- (en) Martin Jansen, « Effects of relativistic motion of electrons on the chemistry of gold and platinum », Solid State Sciences, vol. 7, no 12, , p. 1464-1474 (DOI 10.1016/j.solidstatesciences.2005.06.015, Bibcode 2005SSSci...7.1464J, lire en ligne)