Récepteur alpha activé par les proliférateurs de peroxysomes
Le récepteur alpha activé par les proliférateurs de peroxysomes (en anglais : PPAR-alpha), également connu sous le nom de NR1C1 (récepteur nucléaire de la sous-famille 1, groupe C, membre 1), est une protéine du récepteur nucléaire qui, chez l'homme, est codée par le gène PPARA. Avec le récepteur delta activé par les proliférateurs de peroxysomes et le récepteur gamma activé par les proliférateurs de peroxysomes, le PPAR-alpha fait partie de la sous-famille des récepteurs activés par les proliférateurs de peroxysomes. Il a été le premier membre de la famille PPAR à être cloné en 1990 par Stephen Green et a été identifié comme le récepteur nucléaire d'une classe diverse d'hépatocarcinogènes de rongeurs qui provoque la prolifération des peroxysomes. Son gène est PPARA situé sur le chromosome 22 humain
Fonctions
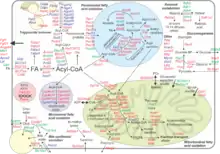
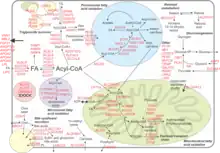
Le PPAR-alpha est un facteur de transcription et un régulateur majeur du métabolisme des lipides dans le foie. Le PPAR-alpha est activé dans des conditions de privation d'énergie et est nécessaire au processus de cétogenèse, une réponse adaptative clé au jeûne prolongé. L'activation des PPAR-alpha favorise l'absorption, l'utilisation et le catabolisme des acides gras par la régulation des gènes impliqués dans le transport des acides gras, la liaison et l'activation des acides gras, et la β-oxydation des acides gras peroxysomaux et mitochondriaux. Le PPAR-alpha est principalement activé par la liaison de ligands. Les ligands synthétiques comprennent les médicaments à base de fibrates, qui sont utilisés pour traiter l'hyperlipidémie, et un ensemble varié d'insecticides, d'herbicides, de plastifiants et de solvants organiques collectivement appelés proliférateurs de peroxysomes. Les ligands endogènes comprennent des acides gras tels que l'acide arachidonique ainsi que d'autres acides gras polyinsaturés et divers composés dérivés d'acides gras tels que certains membres de la famille de l'acide 15-hydroxyicosatétraénoïque des métabolites de l'acide arachidonique, par exemple le 15(S)-HETE, le 15(R)-HETE, et le 15(S)-HpETE et l'acide 13-hydroxyoctadécadiénoïque, un métabolite de l'acide linoléique.
Distribution tissulaire
L'expression de PPAR-alpha est la plus élevée dans les tissus qui oxydent les acides gras à un rythme rapide. Chez les rongeurs, les plus hauts niveaux d'expression de l'ARNm des PPAR-alpha se trouvent dans le foie et les tissus adipeux bruns, suivis du cœur et des reins. Les niveaux d'expression PPAR-alpha les plus bas se trouvent dans l'intestin grêle et le gros intestin, les muscles squelettiques et les glandes surrénales. Le PPAR-alpha humain semble s'exprimer de manière plus égale dans divers tissus, avec une forte expression dans le foie, l'intestin, le cœur et les reins.
Études "Knockout" de ces gènes
Des études utilisant des souris dépourvues de PPAR-alpha fonctionnel indiquent que le PPAR-alpha est essentiel pour l'induction de la prolifération des peroxysomes par un ensemble diversifié de composés synthétiques appelés proliférateurs de peroxysomes. Les souris dépourvues de PPAR-alpha ont également une réponse altérée au jeûne, caractérisée par des perturbations métaboliques majeures, notamment de faibles taux plasmatiques de corps cétoniques, une hypoglycémie et un foie gras.
Pharmacologie
Le PPAR-alpha sert de récepteur cellulaire pour les fibrates, une classe de médicaments utilisés dans le traitement de la dyslipidémie. Les fibres abaissent efficacement les triglycérides sériques et augmentent le taux de cholestérol HDL sérique. Bien que des avantages cliniques du traitement par les fibrates aient été observés, les résultats globaux sont mitigés et ont conduit à des réserves quant à l'application à grande échelle des fibrates pour le traitement des maladies coronariennes, contrairement aux statines. Les agonistes PPAR-alpha peuvent avoir une valeur thérapeutique pour le traitement des maladies hépatiques grasses non alcooliques. Le PPAR-alpha peut également être un site d'action de certains anticonvulsivants.
Gènes ciblés
Le PPAR-alpha régit les processus biologiques en modifiant l'expression d'un grand nombre de gènes cibles. En conséquence, le rôle fonctionnel du PPAR-alpha est directement lié à la fonction biologique de ses gènes cibles. Les études de profilage de l'expression génétique ont indiqué que les gènes cibles PPAR-alpha se comptent par centaines. Les gènes cibles classiques de PPAR-alpha comprennent PDK4, ACOX1 et CPT1. L'analyse de l'expression des gènes à faible et à fort débit a permis de créer des cartes complètes illustrant le rôle du PPAR-alpha en tant que régulateur principal du métabolisme des lipides par la régulation de nombreux gènes impliqués dans divers aspects du métabolisme des lipides. Les cartes, construites pour le foie de souris et le foie humain, placent le PPAR-alpha au centre d'un pôle de régulation ayant un impact sur l'absorption des acides gras et la liaison intracellulaire, l'oxydation mitochondriale et la β-oxydation des acides gras peroxysomaux, la cétogenèse, le renouvellement des triglycérides, la gluconéogenèse et la synthèse/sécrétion de la bile.
Interactions
Il a été démontré que le récepteur alpha activé par les proliférateurs de péroxisomes interagit avec ces derniers :
Références
- Sumanasekera WK, Tien ES, Turpey R, Vanden Heuvel JP, Perdew GH, « Evidence that peroxisome proliferator-activated receptor alpha is complexed with the 90-kDa heat shock protein and the hepatitis virus B X-associated protein 2 », J. Biol. Chem., vol. 278, no 7, , p. 4467–73 (PMID 12482853, DOI 10.1074/jbc.M211261200)
- Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M, « p300 functions as a coactivator for the peroxisome proliferator-activated receptor alpha », J. Biol. Chem., vol. 272, no 52, , p. 33435–43 (PMID 9407140, DOI 10.1074/jbc.272.52.33435)
- Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M, « Identification of nuclear receptor corepressor as a peroxisome proliferator-activated receptor alpha interacting protein », J. Biol. Chem., vol. 274, no 22, , p. 15901–7 (PMID 10336495, DOI 10.1074/jbc.274.22.15901)
- Treuter E, Albrektsen T, Johansson L, Leers J, Gustafsson JA, « A regulatory role for RIP140 in nuclear receptor activation », Mol. Endocrinol., vol. 12, no 6, , p. 864–81 (PMID 9626662, DOI 10.1210/mend.12.6.0123)
Annexes
- Rakhshandehroo M, Hooiveld G, Müller M, Kersten S, « Comparative analysis of gene regulation by the transcription factor PPARalpha between mouse and human. », PLoS ONE, vol. 4, no 8, , e6796 (PMID 19710929, PMCID 2729378, DOI 10.1371/journal.pone.0006796)
- Berger J, Moller DE, « The mechanisms of action of PPARs. », Annu. Rev. Med., vol. 53, , p. 409–35 (PMID 11818483, DOI 10.1146/annurev.med.53.082901.104018)
- Kuenzli S, Saurat JH, « Peroxisome proliferator-activated receptors in cutaneous biology. », Br. J. Dermatol., vol. 149, no 2, , p. 229–36 (PMID 12932225, DOI 10.1046/j.1365-2133.2003.05532.x)
- Mandard S, Müller M, Kersten S, « Peroxisome proliferator-activated receptor alpha target genes. », Cell. Mol. Life Sci., vol. 61, no 4, , p. 393–416 (PMID 14999402, DOI 10.1007/s00018-003-3216-3)
- van Raalte DH, Li M, Pritchard PH, Wasan KM, « Peroxisome proliferator-activated receptor (PPAR)-alpha: a pharmacological target with a promising future. », Pharm. Res., vol. 21, no 9, , p. 1531–8 (PMID 15497675, DOI 10.1023/B:PHAM.0000041444.06122.8d)
- Lefebvre P, Chinetti G, Fruchart JC, Staels B, « Sorting out the roles of PPAR alpha in energy metabolism and vascular homeostasis. », J. Clin. Invest., vol. 116, no 3, , p. 571–80 (PMID 16511589, PMCID 1386122, DOI 10.1172/JCI27989)
- Mukherjee R, Jow L, Noonan D, McDonnell DP, « Human and rat peroxisome proliferator activated receptors (PPARs) demonstrate similar tissue distribution but different responsiveness to PPAR activators. », J. Steroid Biochem. Mol. Biol., vol. 51, nos 3–4, , p. 157–66 (PMID 7981125, DOI 10.1016/0960-0760(94)90089-2)
- Miyata KS, McCaw SE, Patel HV, Rachubinski RA, Capone JP, « The orphan nuclear hormone receptor LXR alpha interacts with the peroxisome proliferator-activated receptor and inhibits peroxisome proliferator signaling. », J. Biol. Chem., vol. 271, no 16, , p. 9189–92 (PMID 8621574, DOI 10.1074/jbc.271.16.9189)
- Chu R, Lin Y, Rao MS, Reddy JK, « Cloning and identification of rat deoxyuridine triphosphatase as an inhibitor of peroxisome proliferator-activated receptor alpha. », J. Biol. Chem., vol. 271, no 44, , p. 27670–6 (PMID 8910358, DOI 10.1074/jbc.271.44.27670)
- Tugwood JD, Aldridge TC, Lambe KG, Macdonald N, Woodyatt NJ, « Peroxisome proliferator-activated receptors: structures and function. », Ann. N. Y. Acad. Sci., vol. 804, , p. 252–65 (PMID 8993548, DOI 10.1111/j.1749-6632.1996.tb18620.x)
- Li H, Gomes PJ, Chen JD, « RAC3, a steroid/nuclear receptor-associated coactivator that is related to SRC-1 and TIF2. », Proc. Natl. Acad. Sci. U.S.A., vol. 94, no 16, , p. 8479–84 (PMID 9238002, PMCID 22964, DOI 10.1073/pnas.94.16.8479)
- Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M, « p300 functions as a coactivator for the peroxisome proliferator-activated receptor alpha. », J. Biol. Chem., vol. 272, no 52, , p. 33435–43 (PMID 9407140, DOI 10.1074/jbc.272.52.33435)
- Inoue I, Shino K, Noji S, Awata T, Katayama S, « Expression of peroxisome proliferator-activated receptor alpha (PPAR alpha) in primary cultures of human vascular endothelial cells. », Biochem. Biophys. Res. Commun., vol. 246, no 2, , p. 370–4 (PMID 9610365, DOI 10.1006/bbrc.1998.8622)
- Treuter E, Albrektsen T, Johansson L, Leers J, Gustafsson JA, « A regulatory role for RIP140 in nuclear receptor activation. », Mol. Endocrinol., vol. 12, no 6, , p. 864–81 (PMID 9626662, DOI 10.1210/mend.12.6.0123)
- Rubino D, Driggers P, Arbit D, Kemp L, Miller B, Coso O, Pagliai K, Gray K, Gutkind S, Segars J, « Characterization of Brx, a novel Dbl family member that modulates estrogen receptor action. », Oncogene, vol. 16, no 19, , p. 2513–26 (PMID 9627117, DOI 10.1038/sj.onc.1201783)
- Yuan CX, Ito M, Fondell JD, Fu ZY, Roeder RG, « The TRAP220 component of a thyroid hormone receptor- associated protein (TRAP) coactivator complex interacts directly with nuclear receptors in a ligand-dependent fashion. », Proc. Natl. Acad. Sci. U.S.A., vol. 95, no 14, , p. 7939–44 (PMID 9653119, PMCID 20908, DOI 10.1073/pnas.95.14.7939)
- Chinetti G, Griglio S, Antonucci M, Torra IP, Delerive P, Majd Z, Fruchart JC, Chapman J, Najib J, Staels B, « Activation of proliferator-activated receptors alpha and gamma induces apoptosis of human monocyte-derived macrophages. », J. Biol. Chem., vol. 273, no 40, , p. 25573–80 (PMID 9748221, DOI 10.1074/jbc.273.40.25573)
- Costet P, Legendre C, Moré J, Edgar A, Galtier P, Pineau T, « Peroxisome proliferator-activated receptor alpha-isoform deficiency leads to progressive dyslipidemia with sexually dimorphic obesity and steatosis. », J. Biol. Chem., vol. 273, no 45, , p. 29577–85 (PMID 9792666, DOI 10.1074/jbc.273.45.29577)
- Masuda N, Yasumo H, Furusawa T, Tsukamoto T, Sadano H, Osumi T, « Nuclear receptor binding factor-1 (NRBF-1), a protein interacting with a wide spectrum of nuclear hormone receptors. », Gene, vol. 221, no 2, , p. 225–33 (PMID 9795230, DOI 10.1016/S0378-1119(98)00461-2)
- Rakhshandehroo M, Sanderson LM, Matilainen M, Stienstra R, Carlberg C, de Groot PJ, Müller M, Kersten S, « Comprehensive analysis of PPARalpha-dependent regulation of hepatic lipid metabolism by expression profiling. », PPAR Res., vol. 2007, , p. 1–13 (PMID 18288265, PMCID 2233741, DOI 10.1155/2007/26839)