Réaction de Michaelis-Arbuzov
La réaction de Michaelis-Arbuzov[1] - [2] est une réaction chimique entre un phosphite et un halogénure d'alkyle qui conduit à la formation d'un phosphonate.
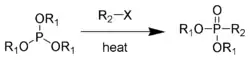
Réaction de Michaelis-Arbuzov
Mécanisme réactionnel
Le doublet non liant du phosphite attaque l'halogénure d'alkyle dans une substitution nucléophile de type SN2 et forme un trialkoxyphosphonium intermédiaire. À chaud, l'anion halogénure attaque un des groupes alkoxy pour former le phosphonate et un halogénure d'alkyle. La force motrice de la réaction est, comme souvent avec le phosphore, la formation d'une liaison P=O.
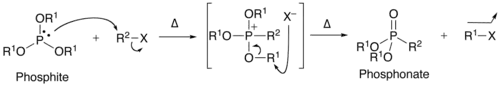
Mécanisme de la réaction de Michaelis-Arbuzov
Il peut y avoir compétition entre l'halogénure d'alkyle utilisé comme réactif et celui produit lors de la réaction. Il est donc préférable de :
- Utiliser un halogénure d'alkyle R2X plus réactif que R1X.
- Utiliser un phosphite (méthyle, éthyle) qui forme un halogénure R1X qui est gazeux à la température de réaction.
- Mener la réaction sous vide de façon à retirer le plus rapidement possible l'halogénure R1X du milieu réactionnel[3].
Références
- (de) A. Michaelis et R. Kaehne, « Ueber das Verhalten der Jodalkyle gegen die sogen. Phosphorigsäureester oder O-Phosphine », Ber. Dtsch. Chem. Ges., vol. 31, no 1, , p. 1048–1055 (ISSN 0365-9496, DOI 10.1002/cber.189803101190, lire en ligne).
- Arbuzov, A. E.; J. Russ. Phys. Chem. Soc. 1906, 38, 687 ; Arbuzov, A. E.; Chem. Zentr. 1906, II, 1639.
- Par exemple, voir (en) M. Saady, L. Lebeau et al., « First use of benzyl phosphites in the Michaelis-Arbuzov reaction synthesis of mono-, di-, and triphosphate analogs », Helv. Chim. Acta, vol. 78, no 3, , p. 670–678 (ISSN 0018-019X, DOI 10.1002/hlca.19950780314).
Liens externes
- Bhattacharya, A. K.; Thyagarajan, G. Chem. Rev. 1981, 81, 415-430. (Review)
- Ford-Moore, A. H.; Perry, B. J. Organic Syntheses, Coll. Vol. 4, p.325 (1963); Vol. 31, p.33 (1951). (Article)
- Nagata, W.; Wakabayashi, T.; Hayase, Y. Organic Syntheses, Coll. Vol. 6, p.448 (1988); Vol. 53, p.44 (1973). (Article)
- Davidsen, S. K.; Phllips, G. W.; Martin, S. F. Organic Syntheses, Coll. Vol. 8, p.451 (1993); Vol. 65, p.119 (1987). (Article)
- Enders, D.; von Berg, S.; Jandeleit, B. Organic Syntheses, Coll. Vol. 10, p.289 (2004); Vol. 78, p.169 (2002). (Article)
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.