Réaction de Dakin-West
La réaction de Dakin-West est une réaction organique transformant un acide aminé en un céto-amide, par action d'un anhydride d'acide et d'une base, typiquement la pyridine[1] - [2] - [3] - [4] - [5]. Elle est nommée d'après Henry Drysdale Dakin et Randolph West. Il est à noter que le produit final est toujours un mélange racémique.
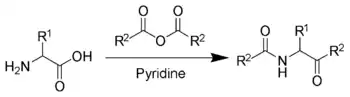
Lorsque la pyridine est utilisée comme solvant et base, il est nécessaire de chauffer le milieu réactionnel à reflux[6]. Cependant, lorsqu'on utilise la 4-diméthylaminopyridine (DMAP) comme catalyseur, la réaction peut avoir lieu à température ambiante[7].
Avec certains acides, cette réaction peut avoir lieu même en l'absence d'un groupe α-aminé.
Mécanisme réactionnel
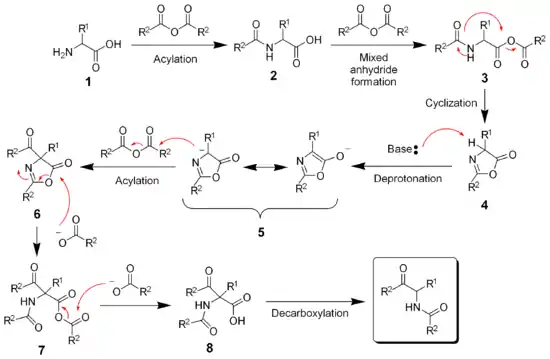 Mécanisme réactionnel de la réaction de Dakin-West
Mécanisme réactionnel de la réaction de Dakin-West
Le mécanisme réactionnel implique l'acylation et l'activation de l'acide (1) pour former un anhydride mixte (3). L'amide va alors servir de nucléophile pour une cyclisation formant une azalactone (4). La déprotonation et l'acylation de cette azalactone forment alors la liaison carbone-carbone recherchée. Consécutivement, l'ouverture du cycle (6) et une décarboxylation donnent le céto-amide final[8] - [9].
Synthèse générale de cétone
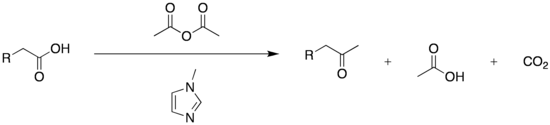
Des variantes modernes de la réaction de Dakin-West permettent de convertir beaucoup d'acides carboxyliques énolisables — et pas seulement les acides aminés — en cétones méthylées correspondantes. Par exemple, les acides carboxyliques β-arylés peuvent être efficacement convertis en cétones β-arylées par traitement avec l'anhydride acétique catalysé à l'aide de 1-méthylimidazole. Cette réactivité est attribuée en partie à la génération in situ d'un acétylimidazolium, puissant agent d'acétylation cationique[10].
Notes et références
- (en) H. D. Dakin et R. West, « A general reaction of amino acids », J. Biol. Chem., vol. 78, , p. 91-104 (ISSN 0021-9258, lire en ligne).
- (en) H. D. Dakin et R. West, « A general reaction of amino acids. II. », J. Biol. Chem., vol. 78, , p. 745-756 (ISSN 0021-9258, lire en ligne).
- (en) H. D. Dakin et R. West, « Some aromatic derivatives of substituted acetylaminoacetones », J. Biol. Chem., vol. 78, , p. 757-764 (ISSN 0021-9258, lire en ligne).
- (en) R. H. Wiley, « The conversion of α-amino acids to oxazoles », J. Org. Chem., vol. 12, no 1, , p. 43–46 (ISSN 0022-3263, DOI 10.1021/jo01165a006).
- (en) G. L. Buchanan, « The Dakin–West reaction », Chem. Soc. Rev., vol. 17, , p. 91-109 (ISSN 0306-0012, DOI 10.1039/CS9881700091).
- (en) R. H. Wiley et O. H. Borum, « 3-acetamido-2-butanone », Org. Synth., vol. 33, , p. 1 (ISSN 0078-6209, DOI 10.15227/orgsyn.033.0001).
- (en) G. Höfle, W. Steglich et al., « 4-Dialkylaminopyridines as Highly Active Acylation Catalysts », Angew. Chem. Int. Ed., vol. 17, no 8, , p. 569–583 (ISSN 1433-7851, DOI 10.1002/anie.197805691).
- (de) R. Knorr et R. Huisgen, « Zum Mechanismus der Dakin-West-Reaktion, I Die Reaktion von N-Acyl-sek.-aminosäuren mit Acetanhydrid », Chem. Ber., vol. 103, no 8, , p. 2598–2610 (ISSN 0009-2940, DOI 10.1002/cber.19701030831).
- (en) N. L. Allinger, G. L. Wang et al., « Kinetic and mechanistic studies of the Dakin-West reaction », J. Org. Chem., vol. 39, no 12, , p. 1730–1735 (ISSN 0022-3263, DOI 10.1021/jo00925a029).
- (en) K.-V. Tran et D. Bickar, « Dakin−West Synthesis of β-Aryl Ketones », J. Org. Chem., vol. 71, no 17, , p. 6640–6643 (ISSN 0022-3263, DOI 10.1021/jo0607966).
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Dakin–West reaction » (voir la liste des auteurs).