Pyrolyse-chromatographie en phase gazeuse-spectrométrie de masse
La pyrolyse couplée à la spectrométrie de masse (Py-CG-SM) est une pyrolyse suivie d'une chromatographie en phase gazeuse-spectrométrie de masse. Cette technique d'analyse chimique repose sur une altération massive par la chaleur, en particulier des structures complexes (polymères, copolymères ou autres analytes complexes non-solubles) ne pouvant pas être directement analysées par chromatographie en phase gazeuse (par manque de volatilité). Cette technique, très polyvalente, est souvent utilisée pour minimiser la préparation d'échantillons et des analyses peuvent se faire sur le terrain avec des systèmes portatifs.
Les hauts polymères figurent parmi les analytes les plus difficiles à analyser car ils possèdent de très hauts poids moléculaires et ne sont pas volatils. D’autres techniques utilisées pour analyser ceux-ci en chimie analytique sont l’analyse thermogravimétrique (TGA), la microscopie électronique à balayage (MEB), la spectroscopie infrarouge à transformée de Fourier (FTIR), la chromatographie d'exclusion stérique (SEC) et la spectrométrie de masse[1].
Rôle de la pyrolyse
La pyrolyse (du grec Pyro, « feu » et lyso, « décomposition ») couplée à la CG a fait ses débuts dans les années 1960. Les deux techniques analytiques furent couplées en 1960 à l’université de Cologne en Allemagne. En 1960, quinze articles étaient publiés sur la Py-CG ; en 1965, quarante articles et en 1970, quatre cents articles[2] - [3]. La pyrolyse consiste à un transfert l’énergie, sous forme de chaleur, à une substance afin d'avoir un changement de composition chimique (décomposition) ou un changement physique (ébullition, fusion).
La dégradation thermique coupe les liaisons chimiques grâce à l'énergie thermique élevée, pour produire des petites molécules volatiles. De nombreux facteurs sont impliqués dans l'analyse Py-CG, par exemple la température, le gradient de température, la durée de l’analyse, les réactions secondaires, la taille de l’échantillon et la vélocité du gaz inerte[2]. La gamme de température souvent utilisée en Py-CG est de 500 à 1 400 °C en présence d’un gaz inerte[3]. La plupart des décompositions thermiques sont dues au bris de molécules polymères de grande taille en leurs monomères, leurs forces relatives étant faibles : un polymère se dégradera en monomère avant de subir des décompositions intra-moléculaires[3]. La fragmentation du polymère est contrôlée par la température, le taux de chauffage en fonction du temps. Or, un contrôle précis des paramètres de chauffage et de la température de l'échantillon est important lors de cette analyse. Il existe deux systèmes de chauffage possibles pour mieux analyser un échantillon : une augmentation graduelle de la température (pyrolyse dans un four) ou un mode impulsion de chaleur par laser ou filament (pyrolyse flash)[3] qui peut augmenter la température d’un échantillon à un taux de 103 à 106 K·s-1[4].
Le support à échantillon utilisé pour ce type d’analyse doit résister à un grand stress dû aux très hautes températures. Un petit tube de quartz est utilisé pour la plupart des analyses Py-CG car il peut résister aux grandes températures requises dans ces analyses.
Chromatographie en phase gazeuse
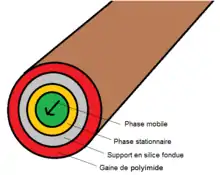
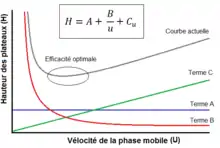
La chromatographie en phase gazeuse est une technique de séparation analytique visant à séparer les analytes de la phase mobile originaires d’une matrice en fonction de leur affinité pour la phase stationnaire de la colonne de chromatographie. Plusieurs effets affecteront la séparation ; les principaux sont la diffusion d'Eddy (en), la diffusion longitudinale, le transfert de masse et la vélocité de la phase mobile. Tous ces termes affecteront la résolution de la séparation (hauteur des plateaux). Ces effets sont regroupés dans l’équation de van Deemter (en).
Les colonnes de chromatographie les plus utilisées en Py-CG-SM sont des phases stationnaires à base de silice fondue (paroi interne recouverte d’un film) car le matériel est relativement inerte, et cette silice est renforcée par une gaine de polyimide (flexible et durable)[3]. Différentes colonnes contenant des phases stationnaires variables sont utilisées pour les CG, dépendamment des analytes et de la température de la pyrolyse. Un choix judicieux de colonne devra être fait pour chaque analyte pour obtenir une résolution optimale des pics. Les principales composantes des phases stationnaires sont composées de polydiméthylsiloxane, de phényle (x %)-diméthylarylène siloxane (100-x %)[5], de polyéthylène glycol et de divinylbenzène[6].
Spectrométrie de masse
La spectrométrie de masse analysera les analytes élués en fonction de leur masse. Ceci permettra de connaitre exactement leur masse molaire et leur nature en fonction de leur rapport masse sur charge (m/z). Un analyseur de masse possède plusieurs composantes : source d’ions, analyseur de masse et détecteur. Tous ces paramètres varieront en fonction de la nature des analytes. La source d’ions la plus utilisée pour les analyses de type Py-CG-SM est l’impact électronique, car ce type d’ionisation vise principalement les petites molécules (H2O, CO2, N2), souvent un des produits présents dans les différentes matrices analysées par cette technique. L’impact électronique produit des ionisations reproductibles et les données peuvent être comparées à des bases de données, permettant d’extraire beaucoup d’informations sur la structure. L’analyseur de masse utilisé lors d’analyse Py-CG-SM varie beaucoup en fonction de la résolution voulue et l’équipement disponible. Certaines expériences utilisent un analyseur de masse quadripolaire, qui sépare les ions sélectivement en fonction de leurs rapports m/z, d’autres utilisent un analyseur à temps de vol, qui analysera le rapport m/z en fonction du temps pris par les ions pour parcourir une certaine distance.
Applications
L’analyse pyrolyse couplée à la chromatographie gazeuse – spectrométrie de masse est principalement utilisée pour l’identification de polymères dans les milieux environnemental, biologique, médical ainsi que l’industrie du caoutchouc. L’analyse de matrices prélevées directement du milieu (dans une forêt, par exemple) ne nécessite pas de séparations préalables avec la technique Py-CG-SM, ce qui sera très représentatif des espèces chimiques présentes. Par exemple, l’analyse d’un échantillon de terre (via pyrolyse thermogravimétrique) pourrait révéler les résines naturelles, la matière organique ainsi que les pesticides, ou identifier les monomères d’un polymère qui se trouve dans une peinture automobile.
Avantages
- Très peu de préparation d’échantillon est nécessaire, qui mène à une économie de temps et de ressources (solvants organiques).
- Les résultats de SM peuvent être comparés à des spectres présents dans une base de données (ex. : MassBank).
- Les échantillons normalement non-analysables en CG-SM peuvent être analysés.
- Les analyses de très petits échantillons (de masse inférieure à un milligramme) sont possibles.
- Les résultats sont très reproductibles.
Désavantages
- Création de radicaux lors de la pyrolyse, ce qui créera des réactions secondaires non-représentatives des produits faisant partie de la matrice initiale.
- La fragmentation supplémentaire via impact électronique est une autre source de fragmentation si l’énergie d’impact (exprimée en électron-volts, symbole eV) n’est pas finement contrôlée.
- Difficulté d’élucider l’ordre des monomères dans les copolymères. Les copolymères aléatoires ne se sépareront pas toujours en monomères mais en dimères, trimères, etc.
Références
- (en) Kursh, P. ; Identification of synthetic polymers and copolymers by analytical pyrolysis – gas chromatography/mass spectrometry, J. Chem. Educ., 2014, 91 (10), p. 1725–1728
- (en) Berezkin, V.G. ; Alishoyev, V.R. ; Nemirovskaya, I.B. ; Gas chromatography of polymers, J. Chro. Lib., vol. 10, 1977, p. 159 (ISBN 0-444-41514-9)
- (en) Kusch, P. ; Pyrolysis-Gas Chromatography/Mass Spectrometry of Polymeric Materials [PDF], Adv. Gas Chro., 2012 (ISBN 978-953-51-0298-4)
- (en) Palumbo, A.W. ; Weimer A.W. ; Heat transfer-limited flash pyrolysis of woody biomass, J. Anal. Appl. Pyrolysis 113 (2015) 474–482
- Améliorez la productivité et la justesse pour votre instrument de CPG/SM [PDF], sur Agilent.com (consulté le 15 décembre 2015)
- (en) Guide d’application d’utilisation des phases stationnaires en CG, sur Agilent.com (consulté le 28 novembre 2015)