Microscopie PALM
La microscopie PALM (en anglais : photo-activated localization microscopy ou microscopie par localisation photoactivée) est une microscopie à fluorescence en champ large permettant de dépasser la limite de diffraction (super-résolue) pour atteindre des résolutions typiques de l'ordre de 20nm [1]. La méthode a été proposée en 2006[2] par Eric Betzig et son équipe, qui a été récompensé par le prix Nobel de chimie 2014 pour ce travail [3].
Le développement de cette technique a été étroitement lié à l'évolution des nouvelles protéines fluorescentes présentant un photochromisme contrôlable, telles la protéine fluorescente verte (GFP).
Principe
La microscopie de fluorescence repose sur un marquage sélectif de l'échantillon avec une molécule fluorescente, par exemple liée par anticorps en immunohistochimie ou en utilisant une protéine génétiquement incluse au gène d'intérêt. Le contraste augmente avec la densité de fluorophores, mais un fluorophore unique peut quand même être vu à l'aide d'un microscope, voire à l'œil nu[4] si le nombre de photons émis est suffisant et le fond assez sombre. Cependant, la résolution d'un microscope est fixée par la capacité à séparer deux points lumineux. Or l'image d'un point lumineux n'est pas ponctuelle, à cause de la diffraction, mais consiste en une tache d'Airy. La résolution est alors limitée par le critère de Rayleigh.
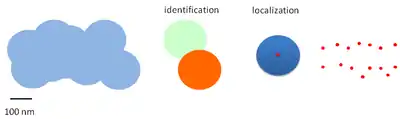
L'idée de la microscopie PALM est de remplacer ce critère de séparation par un critère de localisation de source unique. La résolution au sens strict est donc remplacée par la localisation. Il s'agit alors de contrôler la fluorescence de molécules uniques, par stimulations courtes. Les molécules émettant de la lumière une par une, il est possible de séparer les photons venant de chaque émetteur. Lors d'un processus d'imagerie PALM, on enregistre pour traitement environ 10 000 images contenant les taches d'Airy résultant de l'observation des émetteurs par le microscope [5]. La localisation exacte de la position est alors réalisée par l'ajustement d'une fonction gaussienne en deux dimensions du profil d'émission.
La microscopie STORM est une technique basée sur les mêmes principes, mais utilisant à l'origine des cyanines appariées. Une des molécules de la paire (appelée l'activateur) étant excitée afin de ramener l'autre molécule dans un état de fluorescence.
Références
- (en)The Handbook of nanomedicine sur Google Livres
- E. Betzig, G. H. Patterson, R. Sougrat, O. W. Lindwasser, S. Olenych, J. S. Bonifacino, M. W. Davidson, J. Lippincott-Schwartz, H. F. Hess, « Imaging Intracellular Fluorescent Proteins at Nanometer Resolution », Science, vol. 313, no 5793, , p. 1642–1645 (PMID 16902090, DOI 10.1126/science.1127344, Bibcode 2006Sci...313.1642B)
- (en) , Site Nobel dédié au prix Nobel de Chimie 2014
- W. E. Moerner, D. P. Fromm, « Methods of single-molecule fluorescence spectroscopy and individual fluorescence probes », Review of Scientific Instruments, vol. 74, no 8, , p. 3597–3619 (DOI 10.1063/1.1589587, Bibcode 2003RScI...74.3597M)
- (en)The Handbook of nanomedicine sur Google Livres