Diphosgène
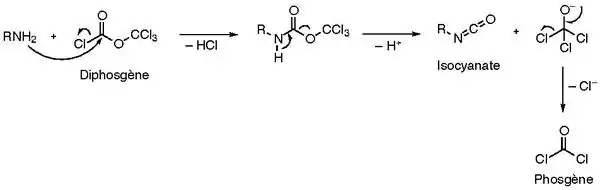
Le diphosgène est un équivalent liquide du phosgène gazeux. Son nom suggère qu'il correspond à deux molécules de phosgène, ce qui est le cas car la réaction d'un nucléophile avec une molécule de diphosgène libère une molécule de phosgène dans le milieu réactionnel :
| Diphosgène | |
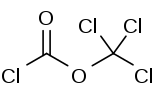
| |
| Diphosgène | |
| Identification | |
|---|---|
| Nom UICPA | carbonochlorurate de trichlorométhyle |
| Synonymes |
chloroformiate de trichlorométhyle |
| No CAS | |
| No ECHA | 100.007.242 |
| No RTECS | LQ7350000 |
| PubChem | 10426 |
| SMILES | |
| InChI | |
| Apparence | liquide |
| Propriétés chimiques | |
| Formule | C2Cl4O2 [Isomères] |
| Masse molaire[1] | 197,832 ± 0,01 g/mol C 12,14 %, Cl 71,68 %, O 16,17 %, |
| Thermochimie | |
| Cp | |
| Précautions | |
| Directive 67/548/EEC | |
 T+ |
|
| Unités du SI et CNTP, sauf indication contraire. | |
 .
.
Le diphosgène a été utilisé comme gaz de combat par l'armée allemande pendant la guerre 1914-1918, il était connu en France sous le nom de supralite et de perstoff en Allemagne.
Articles connexes
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-857-8, 0-88415-858-6 et 0-88415-859-4)
Cet article est issu de wikipedia. Text licence: CC BY-SA 4.0, Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.


