Amobarbital
L'amobarbital (également appelé amylobarbitone ou Amytal sodium) est un ancien médicament barbiturique. Il possède des propriétés sédatives, anxiolytiques et hypnotiques[1].
| Amobarbital | |
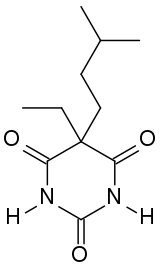
| |
| Données pharmacocinétiques | |
|---|---|
| Excrétion | |
| Identification | |
| No CAS | |
| No ECHA | 100.000.300 |
| Code ATC | N05CA02 |
| DrugBank | 01351 |
Commercialisé pour la première fois en 1923[2] aux États-Unis par Eli Lilly, il est considéré comme un barbiturique à durée d'action intermédiaire.
Son principal fabricant ayant cessé sa fabrication dans les années 1980, le produit est devenu très rare. Il reste cependant fabriqué en Chine[3] où il est parfois vendu illégalement sur internet.
L'utilisation abusive d'amobarbital sous sa forme seule (Amytal en capsules ou Amytal sodium liquide) ou en association avec du sécobarbital (capsules Tuinal) était très répandue aux États-Unis et en Angleterre[4] - [5] - [6] où il était parfois mélangé avec des amphétamines, pour modérer les effets secondaires de celles-ci[2].
Pharmacologie
Analogue du pentobarbital, composé plus répandu, il partage son profil pharmacologique ainsi que son caractère addictif et toxique. Son délai d'action est réputé légèrement plus lent que celle de son analogue[7]. L'amobarbital procurait une sédation rallongée, durant de 6 à 8 heures[8].
Son canal d'action primaire est la modulation positive ainsi que l'activation directe des récepteurs au GABA de type A[9] - [10]. Ces récepteurs, lorsqu'ils sont activés, ont un effet inhibiteur sur la transmission nerveuse en empêchant la dépolarisation membranaire.
Le barbiturique agit également sur d'autres canaux de manière mineure : on note une action inhibitrice de la recapture de l'adénosine, ainsi qu'un antagonisme des récepteurs AMPA et une inhibition de la sécrétion de glutamate[10] - [11].
Comme pour les autres médicaments de sa classe, il présente un potentiel de surdose important, a fortiori lorsque combiné à d'autres sédatifs tels que l'alcool et les narcotiques[12].

Notes et références
- (en) « Amytal Sodium (Amobarbital Sodium Injection): Uses, Dosage, Side Effects, Interactions, Warning », sur RxList (consulté le )
- Francisco López-Muñoz, Ronaldo Ucha-Udabe et Cecilio Alamo, « The history of barbiturates a century after their clinical introduction », Neuropsychiatric Disease and Treatment, vol. 1, no 4, , p. 329–343 (ISSN 1176-6328, PMID 18568113, PMCID 2424120, lire en ligne, consulté le )
- « Barbiturates drug profile | www.emcdda.europa.eu », sur www.emcdda.europa.eu (consulté le )
- (en-GB) Andrew M. Brown, « Winston Churchill's drinking was one thing, but what about his drug-taking? », Daily Telegraph, (ISSN 0307-1235, lire en ligne, consulté le )
- (en) Adam K. Raymond, « PCP, Quaaludes, Black Beauties, Mescaline. What Became of Yesterday's "It" Drugs? », sur The Fix, (consulté le )
- (en) « UNODC - Bulletin on Narcotics - 1962 Issue 2 - 003 », sur United Nations : Office on Drugs and Crime (consulté le )
- (en) Camilla Lieske | Petra A. Volmer, « Illicit Human Drugs »
- « amobarbital », sur www.glowm.com (consulté le )
- (en) Rho, J. M. ; Donevan, S. D. ; Rogawski, M. A. (1996). « Direct activation of GABAA receptors by barbiturates in cultured rat hippocampal neurons » The Journal of physiology 497 (Pt 2): 509–522. PMC 1161000. .
- (en) Wolfgang Löscher et Michael A. Rogawski, « How theories evolved concerning the mechanism of action of barbiturates », Epilepsia, vol. 53, no s8, , p. 12–25 (ISSN 1528-1167, DOI 10.1111/epi.12025, lire en ligne, consulté le )
- Eichi Narimatsu, Tomohisa Niiya, Mikito Kawamata et Akiyoshi Namiki, « [The mechanisms of depression by benzodiazepines, barbiturates and propofol of excitatory synaptic transmissions mediated by adenosine neuromodulation] », Masui. The Japanese Journal of Anesthesiology, vol. 55, no 6, , p. 684–691 (ISSN 0021-4892, PMID 16780077, lire en ligne, consulté le )
- (en) Dymock Rb et James Ra, « Tuinal as a Drug of Abuse », sur The Medical journal of Australia, (PMID 7432291, consulté le )