Acide diaminé
Un acide diaminé est un acide carboxylique portant deux fonctions amine. Il s'agit donc d'un cas particulier d'acides aminés, lesquels correspondent plus généralement aux acides carboxyliques ayant au moins une fonction amine.
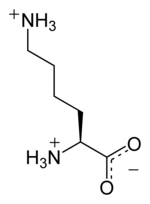
La lysine est un acide diaminé protéinogène, de même que l'asparagine et la glutamine, qui portent une fonction amide. Hormis ces trois composés organiques, il existe un grand nombre d'acides diaminés non protéinogènes assurant une fonction biochimique, comme l'ornithine, qui est un métabolite du cycle de l'urée, ou encore l'acide diaminopimélique, qui est également un acide dicarboxylique et est un constituant essentiel intervenant dans la réticulation du peptidoglycane de la paroi bactérienne chez certaines bactéries.
Des acides diaminés ont été identifiés dans certaines météorites, comme l'acide 2,3-diaminopropionique, ou 3-amino-L-alanine, dans celle de Murchison[1], ainsi que dans des expériences d'irradiation aux ultraviolets de substances simulant la glace cométaire en laboratoire[2]. Ces résultats ont été portés au crédit de théories de la fin du XXe siècle faisant des acides nucléiques peptidiques à base d'acides diaminés les premiers supports de l'information génétique lors de l'apparition de la vie sur Terre[3].
Notes et références
- (en) « Identification of diamino acids in the Murchison meteorite », Proceedings of the National Academy of Sciences of the United States of America, vol. 101, no 25, , p. 9182-9186 (PMID 15194825, PMCID 438950, DOI 10.1073/pnas.0403043101, Bibcode 2004PNAS..101.9182M, lire en ligne)
- (en) « Amino acids from ultraviolet irradiation of interstellar ice analogues », Nature, vol. 416, no 6879, , p. 403-406 (PMID 11919624, DOI 10.1038/416403a, Bibcode 2002Natur.416..403M, lire en ligne)
- (en) Michael Egholm, Ole Buchardt, Leif Christensen, Carsten Behrens, Susan M. Freier, David A. Driver, Rolf H. Berg, Seog K. Kim, Bengt Norden et Peter E. Nielsen, « PNA hybridizes to complementary oligonucleotides obeying the Watson–Crick hydrogen-bonding rules », Nature, vol. 365, no 6446, , p. 566-568 (PMID 7692304, DOI 10.1038/365566a0, Bibcode 1993Natur.365..566E, lire en ligne)