Réaction de Blaise
La réaction de Blaise est une réaction organique de couplage qui permet de former un β-cétoester à partir de zinc métallique, d'un α-bromoester et d'un nitrile[1] - [2] - [3]. La réaction a été publiée pour la première fois par Edmond Blaise en 1901.
Présentation synthétique
Au cours de cette synthèse, une métaloimine intermédiaire est formée, puis hydrolysée pour donner le β-cétoester souhaité[4].
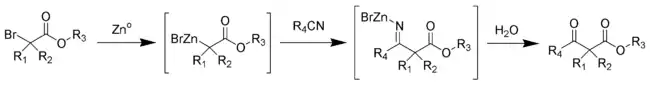
Les esters aliphatiques encombrés donnent en général des rendements plus élevés.
Dans cette réaction, des groupements hydroxyles libres sont tolérés[5] - [6], ce qui est rare lors de réactions faisant intervenir des organométalliques dérivés d'halogénures.
Mécanisme détaillé
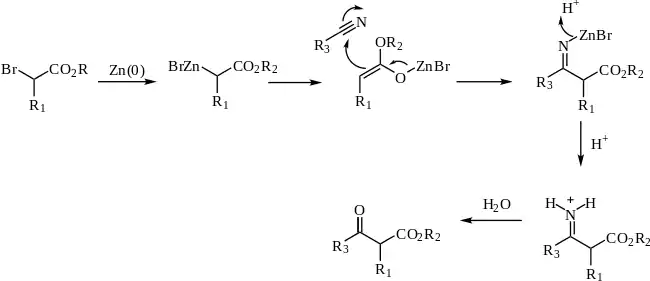
Le mécanisme de la réaction de Blaise passe par la formation d'un organozincique complexe avec le brome en α du carbonyle de l'ester. Cela rend le carbone en α nucléophile, permettant une attaque électrophile du carbone du nitrile. L'azote alors chargé négativement du nitrile interagit avec le monobromure de zinc cationique. Le β-ènaminoester (tautomère de l'imine intermédiaire sur le schéma ci-dessus) est isolé lors d'un traitement du milieu réactionnel par une solution aqueuse à 50 % de K2CO3. Si le β-cétoester est le produit désiré, l'addition d'acide chlorhydrique molaire permet l'hydrolyse du β-ènaminoester en β-cétoester.
Notes et références
Voir aussi
Bibliographie
- Edmond Blaise, « Nouvelles réactions des dérivés organométalliques (II) : Éthers α-alcoyl-β-cétoniques », Comptes rendus hebdomadaires des séances de l'Académie des sciences, vol. 132, , p. 478 (lire en ligne).
- (en) Kenneth L. Rinehart, Jr., « sec-Butyl a-n-Caproylpropionate [Octanoic Acid, 2-methyl-3-Oxo, sec-butyl Ester] », Organic Syntheses, coll. vol. 4, 1963, p. 120 ; vol. 35, 1955, p. 15 (lire en ligne, consulté le ).
- (en) H. Surya Prakash Rao, Shaik Rafi et K. Padmavathy, « The Blaise Reaction », Tetrahedron, vol. 64, , p. 8037-8043.
- (en) James Cason, Kenneth L. Rinehart, Jr. et Stephen D. Thornton, Jr., « The Preparation of β-Keto Esters from Nitriles and α-Bromoesters », The Journal of Organic Chemistry, vol. 18, , p. 1594 (DOI 10.1021/jo50017a022).
- (en) Steven M. Hannick et Yoshito Kishi, « An Improved Procedure for the Blaise Reaction : A Short, Practical Route to the Key Intermediates of the Saxitoxin Synthesis », J. Org. Chem., vol. 48, , p. 3833 (DOI 10.1021/jo00169a053).
- (en) Jiří Pospíšil et István E. Markó, « Total Synthesis of Jerangolid D », Journal of the American Chemical Society, ASAP, (DOI 10.1021/ja0691728).
- (en) Fang-Dao Wang et Jian-Min Yue, « Total Synthesis of (R)-(+)-Kavain via (MeCN)2PdCl2-Catalyzed Isomerization of a cis Double Bond and Sonochemical Blaise Reaction », Synlett, vol. 13, , p. 2077-2079 (DOI 10.1055/s-2005-871953).
Article connexe
Lien externe
- « Blaise Réaction », sur Organic Chemistry Portal, développe le sujet et donne une bibliographie des publications récentes.