Dithionate
L'anion dithionate, de formule brute S2O62−, est un oxoanion de soufre dérivant de l'acide dithionique H2S2O6. Sa formule chimique est parfois écrite de manière semidéveloppée O3SSO32− afin d'en souligner la structure[2].
| Dithionate | |
 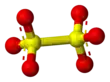 Structure du dithionate |
|
| Identification | |
|---|---|
| Synonymes |
bis(trioxydosulfate)(S--S)(2-), |
| No CAS | |
| PubChem | 3082075 |
| ChEBI | 29209 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | S2O62− |
| Masse molaire[1] | 160,126 ± 0,012 g/mol O 59,95 %, S 40,05 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Les atomes de soufre de l'ion dithionate sont dans l'état d'oxydation +5 du fait de la liaison S–S. Les dithionates forment le plus souvent des composés stables qui ne sont pas facilement oxydés ni réduits. Les oxydants forts les oxydent en sulfates SO42− tandis que les réducteurs forts les réduisent en sulfites SO32− et en dithionites S2O42−[3]. Les solutions aqueuses de dithionate sont stables et peuvent être portées à ébullition sans subir de décomposition[4].
Les cristaux de dithionates exposés aux rayons γ libèrent des ions radicaux SO3−[5]. Les électrons non appariés de l'espèce SO3− peuvent être détectés par résonance paramagnétique électronique et le dithionate de baryum BaS2O6 a été proposé pour la réalisation de dosimètres[6].
Composés
Parmi les composés de l'ion dithionate se trouvent notamment :
- le dithionate de sodium Na2S2O6
- le dithionate de potassium K2S2O6
- le dithionate de baryum BaS2O6
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) NOMENCLATURE OF INORGANIC CHEMISTRY « IUPAC Recommendations 2005 », page 130.
- (en) Norman N. Greenwood, Alan Earnshaw, « Chemistry of the Elements », 2e édition, Butterworth-Heinemann, Oxford, 1997. (ISBN 0080379419)
- (en) F. Albert Cotton, Geoffrey Wilkinson, Carlos A. Murillo, Manfred Bochmann, « Advanced Inorganic Chemistry » 6e édition, Wiley-Interscience, New York, 1999. (ISBN 0-471-19957-5)
- (en) G. S. Murthy, R. L. Eager, K. J. McCallum, « Radiation Chemistry of Dithionates » dans Revue canadienne de chimie, 1971, 49:3733-3738, DOI 10.1139/v71-621
- (en) M. P. Baran, O. A. Bugay, S. P. Kolesnik, V. M. Maksimenko, V. V. Teslenko, T. L. Petrenko et M.-F. Desrosiers, « Barium dithionate as an EPR dosemeter » dans Radiation Protection Dosimetry, 2006 120 202. DOI 10.1093/rpd/nci531