Cryptophane
Un cryptophane est un composé organique appartenant à une famille de composés supramoléculaires (en) découverts en 1981 par Jacqueline Gabard et André Collet[1], et synthétisés et étudiés principalement à des fins de reconnaissance et d'encapsulation moléculaire (en). Une application prometteuse des cryptophanes est l'encapsulation pour le stockage de l'hydrogène en vue d'être utilisé par des véhicules propulsés à l'aide d'une pile à combustible. Ils peuvent également être utilisés en chimie organique pour contenir un milieu réactionnel permettant des réactions chimiques qu'il serait autrement impossible à réaliser dans les conditions normales. Enfin, leurs propriétés remarquables de reconnaissance moléculaire permettent d'envisager de les utiliser pour étudier comment les molécules organiques se lient aux substrats, notamment en vue d'applications biologiques et biochimiques.
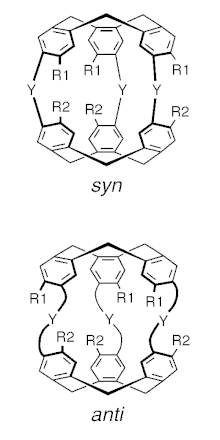
Les cages des cryptophanes sont constituées de deux unités [1.1.1]–orthocyclophane[2] (cyclotrivératrylène, ou CTV) en forme de coupelle liées par trois « ponts » (espaceurs, notés Y) et possédant divers substituants, notés R1 et R2, sur les cycles aromatiques des deux unités CTV. La plupart des cryptophanes présentent deux formes diastéréoisomères syn et anti distinguées par leur type de symétrie. L'ensemble de ces paramètres — Y, R1, R2 et diastéréoisomérie — permet de faire varier les caractéristiques géométriques et chimiques de la cage généralement hydrophobe formée par ces molécules, permettant d'encapsuler spécifiquement un large éventail de petites molécules, voire de réactions chimiques.
La dénomination des cryptophanes, en fonction de leurs caractéristiques Y, R1, R2 et de leur diastéréoisomérie syn ou anti, est la suivante[2] :
| Structure | Dénomination | ||||
|---|---|---|---|---|---|
| Ponts Y | R1 | R2 | anti | syn | Publication |
| 3 × O(CX2)2O, où X représente H ou D | OCX3 | OCX3 | A | Brotin et al.[3] | |
| 3 × O(CX2)2O | OCH2CO2H | OCH2CO2H | A3 | ||
| 3 × O(CX2)2O | OCH3 | H | C | D | |
| 3 × O(CH2)3O | OCH3 | OCH3 | E | F | |
| 3 × O(CH2)3O | OCH2CO2H | OCH2CO2H | E3 | ||
| 3 × O(CH2)5O | OCH3 | OCH3 | O | P | |
| 3 × O(CH2)5O | OCH2CO2H | OCH2CO2H | O3 | ||
| 3 × OCH2–(C≡C–)2CH2O | CH3 | CH3 | γ (gamma) | δ (delta) | |
| 2 × O(CH2)2O, 1 × O(CH2)3O | OCH3 | OCH3 | 223 | ||
| 2 × O(CH2)3O, 1 × O(CH2)2O | OCH3 | OCH3 | 233 | ||
| 2 × O(CH2)2O, 1 × O(CH2)4O | OCH3 | OCH3 | 224 | ||
Notes et références
- (en) Jacqueline Gabard et André Collet, « Synthesis of a (D3)-bis(cyclotriveratrylenyl) macrocage by stereospecific replication of a (C3)-subunit », Journal of the Chemical Society, Chemical Communications, no 21, , p. 1137-1139 (lire en ligne) DOI 10.1039/C39810001137
- (en) Holman, K. Travis Holman, « Cryptophanes: molecular containers », Encyclopedia of Supramolecular Chemistry, 2004, p. 340-348.
- (en) Brotin, T.; Devic, T.; Lesage, A.; Emsley, L.; Collet, A., « Synthesis of deuterium-labeled cryptophane-A and investigation of Xe@Cryptophane complexation dynamics by 1D-EXSY NMR experiments », Chemistry - a European Journal, vol. 7, no 7, , p. 1561–1573 (DOI 10.1002/1521-3765(20010401)7:7<1561::AID-CHEM1561>3.0.CO;2-9)