Arylcyclohexylamine
Les arylcyclohexylamines, aussi appelées arylcyclohexamines ou arylcyclohexanamines, sont une famille de composés chimiques utilisés en pharmacologie et comme drogues de synthèse.

Histoire

La phéncyclidine (PCP) a été la première arylcyclohexylamine connue en tant qu'agent anesthésique, mais plusieurs autres arylcyclohexylamines ont été décrites avant la PCP dans la littérature scientifique, à commencer par la PCA (1-phénylcyclohexane-1-amine) dont la synthèse a été publiée pour la première fois en 1907. La PCE (en) a été découverte en 1953, puis la PCMo en 1954 qui fut décrite comme un puissant sédatif[1]. Les arylcyclohexylamines ont été beaucoup étudiées comme anesthésiques à Parke-Davis, d'abord avec la PCP en 1956, puis avec son analogue, la kétamine[1]. Les années 1970 voient le début de l'usage illicite de ces substances, en particulier la PCP, comme drogues récréatives, du fait de leurs propriétés hallucinogènes dissociatives, ainsi qu'euphorisantes. Depuis, cette classe de substances a été étendue et diversifiée par la recherche scientifique avec le développement d'agents stimulants, analgésiques et neuroprotecteurs, ainsi que par la chimie clandestine dans la recherche de nouvelles drogues récréatives parmi lesquelles la méthoxétamine (ou MXE) est la plus connue.
Propriétés physico-chimiques
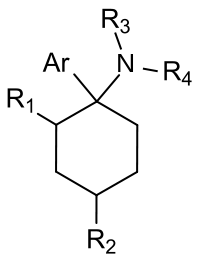
Un arylcyclohexylamine est composé d'un groupe cyclohexylamine lié à un groupe aryle parfois substitué ; groupe lié au carbone qui porte le groupe amine. Le groupe aryle ainsi que le cycle hexyle peuvent être substitués de même que le groupe amine.
Pharmacologie
Les arylcyclohexylamines possèdent des propriétés variées : antagonistes des récepteurs NMDA[2] - [3], inhibiteurs de la recapture de dopamine[4], et agonistes des récepteurs opioïdes μ[5]. En outre, des propriétés agonistes des récepteurs σ [6], antagonistes des récepteurs nACh [7] et agonistes des récepteurs dopaminergiques D2[8] ont été décrites pour certains agents de cette classe. L'antagonisme aux récepteurs NMDA est responsable des propriétés anesthésiques, anticonvulsiviantes, neuroprotectrices, ainsi que de l'effet psychique dit dissociatif ; l'inhibition de la recapture de dopamine induit des effets stimulant et euphorisant, ainsi que des symptômes psychotiques à hautes doses ; et l'activation des récepteurs opioïdes μ apporte des effets analgésiques et euphorisants. La stimulation des récepteurs σ et D2 pourrait aussi contribuer aux effets hallucinogènes de type délirant[8].
Ces agents sont polyvalents, avec un large éventail d'activités pharmacologiques possibles en fonction des modifications chimiques apportées aux composés de base. La variété dans le choix des substitutions permet d'obtenir des molécules avec un profil pharmacologique "sur-mesure". Par exemple, la BTCP est un inhibiteur sélectif de la recapture de dopamine[4], la kétamine est principalement un antagoniste des récepteurs NMDA, le BDPC est un agoniste des récepteurs opioïdes μ très puissant[9] et le PRE-084 est un agoniste sélectif des récepteurs σ[10]. Ainsi, des profils pharmacologiques radicalement différents sont possibles grâce à différentes combinaisons structurelles.
Liste des arylcyclohexylamines
| Nom | Substituant aryle | N | Anneau cyclohexyl |
|---|---|---|---|
| PCA[11] | phényle | NH2 | - |
| PCM[11] | phényle | méthylamino | - |
| Éticyclidine (PCE) | phényle | éthylamino | - |
| PCPr[12] | phényle | n-propylamino | - |
| PCiP | phényle | isopropylamino | - |
| PCBu | phényle | n-butylamino | - |
| PCEOH | phényle | hydroxyéthylamino | - |
| PCMEA[13] | phényle | méthoxyéthylamino | - |
| PCEEA | phényle | éthoxyéthylamino | - |
| PCMPA | phényle | méthoxypropylamino | - |
| PCDM[11] | phényle | diméthylamino | - |
| Diéticyclidine | phényle | diéthylamino | - |
| 2-HO-PCP[2] | phényle | pipéridine | 2-hydroxy |
| 2-Me-PCP[14] | phényle | pipéridine | 2-méthyle |
| 2-MeO-PCP[15] | phényle | pipéridine | 2-méthoxy |
| 2-Céto-PCP | phényle | pipéridine | 2-céto |
| 2-Céto-PCE | phényle | éthylamino | 2-céto |
| 4-Méthyl-PCP | phényle | pipéridine | 4-méthyle |
| 4-Céto-PCP | phényle | pipéridine | 4-céto |
| 2-Cl-PCP | o-chlorophényle | pipéridine | - |
| 3-F-PCP[16] | m-fluorophényle | pipéridine | - |
| 3-Me-PCP[17] | m-méthylphényle | pipéridine | - |
| 3-NH2-PCP | m-aminophényle | pipéridine | - |
| 3-HO-PCP | m-hydroxyphényle | pipéridine | - |
| 3-MeO-PCP | m-méthoxyphényle | pipéridine | - |
| 3-MeO-PCE | m-méthoxyphényle | éthylamino | - |
| 3-MeO-PCPr | m-méthoxyphényle | n-propylamino | - |
| 3-MeO-PCPy[17] | m-méthoxyphényle | pyrrolidine | - |
| 4-HO-PCP | p-hydroxyphényle | pipéridine | - |
| Méthoxydine (4-MeO-PCP) | p-méthoxyphényle | pipéridine | - |
| p-F-PCP[16] | p-fluorophényle | pipéridine | - |
| Arkétamine | o-chlorophényle | méthylamino | 2-céto |
| Deschlorokétamine | phényle | méthylamino | 2-céto |
| Eskétamine | o-chlorophényle | méthylamino | 2-céto |
| Éthkétamine | o-chlorophényle | éthylamino | 2-céto |
| Kétamine | o-chlorophényle | méthylamino | 2-céto |
| Méthoxykétamine | o-méthoxyphényle | méthylamino | 2-céto |
| Fluorokétamine | o-fluorophényle | méthylamino | 2-céto |
| Bromokétamine | o-bromophényle | méthylamino | 2-céto |
| Méthoxétamine | m-méthoxyphényle | éthylamino | 2-céto |
| Phéncyclidine (PCP) | phényle | pipéridine | - |
| PC3MP | phényle | 3-méthylpipéridine | - |
| PC4MP | phényle | 4-méthylpipéridine | - |
| Rolicyclidine (PCPy) | phényle | pyrrolidine | - |
| PCDMPy | phényle | 3,3-diméthylpyrrolidine | - |
| PCMo | phényle | morpholine | - |
| DPD | diphényle | éthylpiperidine | - |
| Méthoxy-PCM[18] | o-méthoxyphényle | morpholine | - |
| Méthyl-PCM[19] | p-méthylphényle | morpholine | - |
| Hydroxy-méthyl-PCM | 2-méthyl-4-hydroxyphényle | morpholine | - |
| TCM | 2-thiényle | méthylamino | - |
| TCE | 2-thiényle | éthylamino | - |
| Ténocyclidine (TCP) | 2-thiényle (furane ?) | pipéridine | - |
| TCPy | 2-thiényle | pyrrolidine | - |
| Tilétamine | 2-thiényle | éthylamino | 2-céto |
| Gacyclidine | 2-thiényle | pipéridine | 2-méthyle |
| BDPC | p-bromophényle | diméthylamino | 4-phénéthyl-4-hydroxy |
| Dimétamine | p-méthylphényle | diméthylamino | 4-céto |
| BTCP[20] | benzothiophène-2-yle | pipéridine | - |
| PRE-084 | phényle | morpholinyléthylcarboxylate | - |
Notes et références
- H. Morris et J. Wallach, « From PCP to MXE: a comprehensive review of the non-medical use of dissociative drugs », Drug Testing and Analysis, vol. 6, nos 7-8, , p. 614–32 (PMID 24678061, DOI 10.1002/dta.1620, lire en ligne)
- A. Ahmadi et A. Mahmoudi, « Synthesis and biological properties of 2-hydroxy-1-(1-phenyltetralyl)piperidine and some of its intermediates as derivatives of phencyclidine », Arzneimittel-Forschung, vol. 55, no 9, , p. 528–532 (PMID 16229117, DOI 10.1055/s-0031-1296900)
- A. Ahmadi, M. Khalili, R. Hajikhani et M. Naserbakht, « New morpholine analogues of phencyclidine: Chemical synthesis and pain perception in rats », Pharmacology Biochemistry and Behavior, vol. 98, no 2, , p. 227–233 (PMID 21215770, DOI 10.1016/j.pbb.2010.12.019)
- I. Chaudieu, Vignon, Chicheportiche, Kamenka, Trouiller et Chicheportiche, « Role of the aromatic group in the inhibition of phencyclidine binding and dopamine uptake by PCP analogs », Pharmacology, Biochemistry, and Behavior, vol. 32, no 3, , p. 699–705 (PMID 2544905, DOI 10.1016/0091-3057(89)90020-8)
- Y. Itzhak et Simon, « A novel phencyclidine analog interacts selectively with mu opioid receptors », The Journal of Pharmacology and Experimental Therapeutics, vol. 230, no 2, , p. 383–386 (PMID 6086884)
- X. S. He, L. P. Raymon, M. V. Mattson, M. E. Eldefrawi et B. R. De Costa, « Synthesis and biological evaluation of 1-1-(2-benzobthienyl)cyclohexylpiperidine homologues at dopamine-uptake and phencyclidine- and sigma-binding sites », Journal of Medical Chemistry, vol. 36, no 9, , p. 1188–1193 (PMID 8098066, DOI 10.1021/jm00061a009)
- V. A. Eterović, R. Lu, A. E. Eakin, A. D. Rodríguez et P. A. Ferchmin, « Determinants of phencyclidine potency on the nicotinic acetylcholine receptors from muscle and electric organ », Cellular and molecular neurobiology, vol. 19, no 6, , p. 745–757 (PMID 10456235)
- P. Seeman, F. Ko et T. Tallerico, « Dopamine receptor contribution to the action of PCP, LSD and ketamine psychotomimetics », Molecular Psychiatry, vol. 10, no 9, , p. 877–883 (PMID 15852061, DOI 10.1038/sj.mp.4001682)
- (en) D. Lednicer et P. F. Vonvoigtlander, « 4-(p-Bromophenyl)-4-(dimethylamino)-1-phenethylcyclohexanol, an extremely potent representative of a new analgesic series », Journal of Medicinal Chemistry, vol. 22, no 10, , p. 1157–1158 (PMID 513062, DOI 10.1021/jm00196a001)
- T. Maurice, T. P. Su, D. W. Parish, T. Nabeshima et A. Privat, « PRE-084, a sigma selective PCP derivative, attenuates MK-801-induced impairment of learning in mice », Pharmacology, Biochemistry, and Behavior, vol. 49, no 4, , p. 859–869 (PMID 7886099, DOI 10.1016/0091-3057(94)90235-6)
- DOI 10.1021/jm00167a027
- C. Sauer, F. Peters, R. Staack, G. Fritschi et H. Maurer, « Metabolism and toxicological detection of a new designer drug, N-(1-phenylcyclohexyl)propanamine, in rat urine using gas chromatography-mass spectrometry », Journal of Chromatography A, vol. 1186, nos 1–2, , p. 380–390 (PMID 18035363, DOI 10.1016/j.chroma.2007.11.002)
- C. Sauer, F. Peters, A. Schwaninger, M. Meyer et H. Maurer, « Investigations on the cytochrome P450 (CYP) isoenzymes involved in the metabolism of the designer drugs N-(1-phenyl cyclohexyl)-2-ethoxyethanamine and N-(1-phenylcyclohexyl)-2-methoxyethanamine », Biochemical pharmacology, vol. 77, no 3, , p. 444–450 (PMID 19022226, DOI 10.1016/j.bcp.2008.10.024)
- M. A. Iorio, L. Tomassini, M. V. Mattson, C. George et A. E. Jacobson, « Synthesis, stereochemistry, and biological activity of the 1-(1-phenyl-2-methylcyclohexyl)piperidines and the 1-(1-phenyl-4-methylcyclohexyl)piperidines. Absolute configuration of the potent trans-(-)-1-(1-phenyl-2-methylcyclohexyl)piperidine », Journal of Medicinal Chemistry, vol. 34, no 8, , p. 2615–2623 (PMID 1875352, DOI 10.1021/jm00112a041)
- A. Ahmadi et A. Mahmoudi, « Synthesis with improved yield and study on the analgesic effect of 2-methoxyphencyclidine », Arzneimittel-Forschung, vol. 56, no 5, , p. 346–350 (PMID 16821645, DOI 10.1055/s-0031-1296732)
- DOI 10.1016/S0022-1139(01)00565-6
- J. Wallach, G. D. Paoli, A. Adejare et S. D. Brandt, « Preparation and analytical characterization of 1-(1-phenylcyclohexyl)piperidine (PCP) and 1-(1-phenylcyclohexyl)pyrrolidine (PCPy) analogues », Drug Testing and Analysis, vol. 6, nos 7–8, , p. 633–50 (PMID 23554350, DOI 10.1002/dta.1468)
- Ahmadi A, Khalili M, Hajikhani R, Naserbakht M, « New morpholine analogues of phencyclidine: chemical synthesis and pain perception in rats », Pharmacology, Biochemistry, and Behavior, vol. 98, no 2, , p. 227–33 (PMID 21215770, DOI 10.1016/j.pbb.2010.12.019)
- Ahmadi A, Khalili M, Hajikhani R, Naserbakht M, « Synthesis and determination of acute and chronic pain activities of 1-[1-(4-methylphenyl) (cyclohexyl)] morpholine as a new phencyclidine derivative in rats », Arzneimittel-Forschung, vol. 61, no 2, , p. 92–7 (PMID 21428243, DOI 10.1055/s-0031-1296173)
- J. Vignon, V. Pinet, C. Cerruti, J. M. Kamenka et R. Chicheportiche, « 3HN-1-(2-benzo(b)thiophenyl)cyclohexylpiperidine (3HBTCP): A new phencyclidine analog selective for the dopamine uptake complex », European Journal of Pharmacology, vol. 148, no 3, , p. 427–436 (PMID 3384005, DOI 10.1016/0014-2999(88)90122-7)