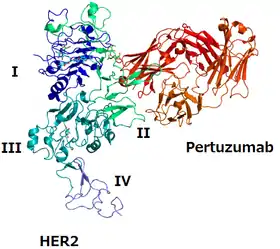
Pertuzumab
Le pertuzumab (commercialisé sous le nom de Perjeta) est un anticorps monoclonal développé par Genentech pour le traitement des cancers du sein HER2-positifs, en combinaison avec le trastuzumab et le docetaxel[1]. En se liant à HER2, il inhibe la dimérisation de la protéine HER2 avec d'autres récepteurs HER, ce qui contribue à ralentir la croissance tumorale[2].
Essais cliniques
Des essais cliniques de phase précoce concernant l'efficacité du pertuzumab pour le traitement des cancers de la prostate, du sein et des ovaires ont montré un succès limité[3].
L'association du pertuzumab au trastuzumab et au docetaxel, comparée à un placebo associé au trastuzumab et au docetaxel, utilisé en première ligne de traitement de cancers du sein HER2-positifs métastatiques, a significativement prolongé la survie sans progression, sans augmentation des effets toxiques cardiaques selon les résultats de l'essai clinique de phase III randomisé en double-aveugle CLEOPATRA[4].
L'administration intraveineuse de pertuzumab est actuellement évaluée chez des patients atteints d'un cancer du sein dans les essais cliniques suivants : MARIANNE (cancer du sein avancé), NEOSPHERE (cancer du sein précoce), TRYPHAENA (cancer du sein HER2-positif de stade II/III) et APHINITY (cancer du sein HER2-positif non métastatique)[4].
Références
- http://www.gene.com/download/pdf/perjeta_prescribing.pdf
- Johann S. de Bono, J Bellmunt, G Attard, JP Droz, K Miller, A Flechon, C Sternberg, C Parker, G Zugmaier, V. Hersberger-Gimenez, L. Cockey, M. Mason et J. Graham, « Open-Label Phase II Study Evaluating the Efficacy and Safety of Two Doses of Pertuzumab in Castrate Chemotherapy-Naive Patients With Hormone-Refractory Prostate Cancer », Journal of Clinical Oncology, vol. 25, no 3, , p. 257–262 (PMID 17235043, DOI 10.1200/JCO.2006.07.0888)
- Genentech press release - May 15, 2005
- Baselga J, Cortés J, Kim SB, and the CLEOPATRA Study Group. Pertuzumab plus trastuzumab plus docetaxel for metastatic breast cancer. N Engl J Med 2012 Jan 12; 366 (2): 109-19. Link text