Cycle catalytique
En chimie, un cycle catalytique est un terme désignant un mécanisme réactionnel à plusieurs étapes impliquant un catalyseur[1]. Le cycle catalytique est la principale façon de décrire le rôle des catalyseurs en biochimie, chimie organométallique, science des matériaux, etc. Souvent, de tels cycles montrent la conversion d'un précatalyseur en catalyseur. Comme les catalyseurs sont régénérés, les cycles catalytiques sont habituellement écrits comme une séquence de réactions chimiques en forme de boucle. Dans de telles boucles, l'étape initiale implique la liaison d'un ou plusieurs réactifs avec le catalyseur, et l'étape finale est la formation du produit et la régénération du catalyseur.
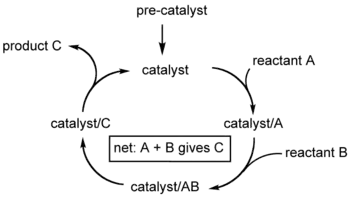
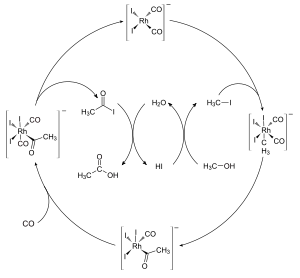
Un cycle catalytique n'est pas nécessairement un mécanisme réactionnel en entier. Par exemple, on peut avoir détecté un intermédiaire réactionnel, tout en ne sachant pas par quel mécanisme la réaction s'est produite.
Les cycles catalytiques ont aussi un rôle important en chimie atmosphérique, par exemple dans les réactions menant à la destruction de la couche d'ozone. L'interaction complexe entre différents régimes, impliquant également des cycles nuls qui n'ont pas d'effet global, détermine le taux de production et de destruction de nombreux composants atmosphériques.
Catalyseur sacrificiel
Souvent un catalyseur dit « sacrificiel » fait également partie du système de réaction dans le but de régénérer le catalyseur vrai pour chaque cycle. Comme son nom l'indique, le catalyseur sacrificiel n'est pas régénéré mais irréversiblement consommé, ce qui correspond au contraire d'un catalyseur. Ce composé sacrificiel est également connu comme catalyseur stœchiométrique lorsqu'il est ajouté en quantité stœchiométrique par rapport au réactif principal. Généralement, le vrai catalyseur est une molécule complexe et coûteuse et est ajouté en quantité aussi faible que possible. Le catalyseur sacrificiel ou stœchiométrique se doit par contre d'être abondant et peu coûteux.
Les catalyseurs sacrificiels sont aussi généralement plus précisément désignés par leur véritable rôle dans le cycle catalytique, par exemple en tant que réducteur, oxydant terminal ou amorceur.
Notes et références
- M. Albert Vannice, Kinetics of catalytic reactions, 2005
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Catalytic cycle » (voir la liste des auteurs).